Рыбий жир: не такой уж и полезный, как казалось

Несмотря на постоянное развитие фармакологии и традиционной медицины, народные средства и пищевые добавки продолжают оставаться популярными. Многие из них захватывают внимание людей своей натуральностью, чудодейственными свойствами и абсолютной безопасностью для организма. Проблема в том, что эти заявления часто не подкреплены практическими доказательствами. Ученые из Медицинского университета Южной Каролины (США) провели исследование, в котором установили, что рыбий жир обладает рядом весьма негативных для мозга человека свойств. Какие тесты проводились, что они показали, и есть ли в рыбьем жире польза помимо обнаруженного вреда? Ответы на эти вопросы мы найдем в докладе ученых.
Основа исследования
Черепно-мозговая травма (ЧМТ или TBI от traumatic brain injury), часто называемая «тихой эпидемией», остается одной из ведущих причин смерти и длительной инвалидности во всем мире, непропорционально затрагивая молодых людей и стареющее население. Хотя повторяющиеся легкие TBI (rmTBI от repetitive mild TBI) часто считаются доброкачественными, все больше данных свидетельствует о том, что даже субклинические травмы могут инициировать хронический каскад нейроваскулярных повреждений, который сохраняется в течение десятилетий, существенно повышая риск хронической травматической энцефалопатии (CTE от chronic traumatic encephalopathy) и деменции. Несмотря на распространенность и долгосрочные последствия, эффективных терапевтических стратегий для остановки или обращения вспять цереброваскулярной деградации, связанной с черепно-мозговой травмой, не существует, что делает пострадавших уязвимыми для многолетнего прогрессирующего снижения когнитивных функций.
Недавние исследования показывают, что способность к восстановлению цереброваскулярной функции не является однородной, а зависит от скоординированных действий эндотелиальных клеток микрососудов головного мозга (BMVEC от brain microvascular endothelial cell) и ремоделирования внеклеточного матрикса (ECM от extracellular matrix), которые вместе играют центральную роль в организации восстановления после черепно-мозговой травмы.
Сосудистая сеть головного мозга, протяженностью более 600 километров, является критически важной инфраструктурой для метаболизма головного мозга, доставки кислорода [1] и выведения отходов. После черепно-мозговой травмы эта цереброваскулярная система особенно восприимчива к повреждениям: до 50% выживших в долгосрочной перспективе демонстрируют стойкую цереброваскулярную патологию. Ангиогенез, определяемый как образование новых сосудов из существующих капилляров, является ключевым регенеративным ответом, поддерживающим восстановление тканей и сохранение целостности нейроваскулярной единицы (NVU от neurovascular unit). Этот процесс жестко регулируется динамическим взаимодействием между эндотелиальными клетками костного мозга (BMVEC), составом внеклеточного матрикса (ECM) и локальными метаболическими сигналами. Однако нарушения энергетического метаболизма эндотелия или сигнальных путей могут препятствовать регенерации сосудов и способствовать долгосрочной дисфункции и нейродегенеративным процессам. Понимание того, как эти клеточные и метаболические факторы формируют регенеративный ответ, имеет решающее значение для разработки целенаправленных вмешательств при травмах головного мозга.
Полиненасыщенные жирные кислоты омега-3 (PUFA от polyunsaturated fatty acid), полученные из рыбьего жира (FO от fish oil), в частности эйкозапентаеновая кислота (EPA от eicosapentaenoic acid) и докозагексаеновая кислота (DHA от docosahexaenoic acid), являются одними из наиболее широко используемых пищевых добавок для поддержания здоровья организма и головного мозга. В отличие от DHA, которая является основным структурным компонентом нейронных мембран, EPA демонстрирует ограниченное включение в мембраны и, как сообщается, влияет на когнитивные функции в определенных условиях, таких как дисбаланс в питании или дефицит кофакторов. Хотя PUFA омега-3 широко известны своими нейропротекторными свойствами, некоторые исследования предполагают, что их эффекты могут варьироваться в зависимости от баланса липидных компонентов, продолжительности воздействия и физиологического контекста, особенно в условиях воспаления или травмы. Хотя несколько исследований показали, что PUFA омега-3 могут поддерживать стабильность сосудов в определенных условиях, другие предполагают, что специфические липидные медиаторы, включая EPA и ее производные, могут модулировать ангиогенные реакции [2] в зависимости от дозы и контекста. Тем не менее взаимосвязь между длительным потреблением омега-3 и цереброваскулярной адаптацией после травмы головного мозга остается недостаточно изученной, особенно с учетом растущей распространенности пищевых добавок среди людей с неврологической уязвимостью.
Для восполнения этого пробела в знаниях ученые внедрили циклический режим питания с добавлением FO, разработанный для имитации прерывистых моделей потребления омега-3, в сочетании с повторяющейся моделью черепно-мозговой травмы легкой степени тяжести (rlmTBI от less-than-mild TBI), которая не вызывает долгосрочных нарушений у животных, содержащихся на контрольных диетах. Эта сенсибилизированная экспериментальная структура позволяет выявлять тонкие изменения в устойчивости цереброваскулярной системы, которые в противном случае могли бы остаться незамеченными. Используя интегративный подход, охватывающий анализ in vivo, in vitro и тканей человека, было показано, что устойчивое обогащение EPA в головном мозге происходит без изменения системных метаболических параметров, и что этот церебральный резервуар избирательно истощается после rlmTBI, что указывает на преимущественное задействование EPA во время реакции на травму. В этом контексте хроническое обогащение EPA было связано с нарушением восстановления сосудов, ремоделирования нейроваскулярных единиц и задержкой когнитивного восстановления. В условиях культивирования эндотелиальных клеток цереброваскулярной системы, благоприятных для метаболизма и имитирующих изменение использования субстратов после травмы, EPA, но не DHA, снижала ангиогенную способность и способность к заживлению ран, ослабляла когезию эндотелия и активировала пути распознавания липидов, что согласуется с данными транскриптомики коры головного мозга. Наконец, посмертное исследование тканей цереброваскулярной эпителиальной ткани выявило сходные признаки дисбаланса полиненасыщенных жирных кислот, сосудистой нестабильности и транскрипционных признаков измененного метаболизма жирных кислот и подавленного ангиогенеза в пораженной коре головного мозга. В совокупности эти данные свидетельствуют о том, что длительное воздействие EPA представляет собой контекстно-зависимую метаболическую уязвимость, способную снизить устойчивость цереброваскулярной системы после травмы головного мозга.
Результаты исследования
Длительное употребление рыбьего жира приводит к аномальному накоплению EPA
Длинноцепочечные n-3 полиненасыщенные жирные кислоты, в частности EPA и DHA, широко признаны в качестве важнейших регуляторов нейрососудистого здоровья и метаболического гомеостаза. Тем не менее несмотря на их широкую терапевтическую привлекательность, долгосрочные последствия длительного обогащения рациона n-3 PUFA для метаболизма липидов в головном мозге остаются невыясненными. В исследуемой модели длительное потребление n-3 PUFA, полученных из рыбьего жира, привело к заметному накоплению неэтерифицированной EPA в головном мозге в условиях гомеостаза, и этот пул избирательно уменьшался после повторных легких травм, что указывает на ранее неидентифицированную форму липидной чувствительности. Хотя этот сдвиг на первый взгляд кажется парадоксальным в свете давно устоявшегося мнения о том, что метаболизм жирных кислот в головном мозге относительно ограничен, недавние исследования показывают, что здоровый мозг, особенно астроциты [3], может окислять жирные кислоты при определенных условиях. Эти данные позволяют предположить, что наблюдаемая картина отражает контекстно-зависимое использование липидных запасов, а не противоречие основным метаболическим принципам. Поскольку длинноцепочечные полиненасыщенные жирные кислоты, такие как EPA и DHA, поступают в организм преимущественно с пищей, а их эндогенное производство ограничено из-за неэффективного преобразования альфа-линоленовой кислоты, ученые изучили, как добавки рыбьего жира влияют на циркулирующие и мозговые запасы неэтерифицированных жирных кислот в исходном состоянии и после травмы.
Изображение №1
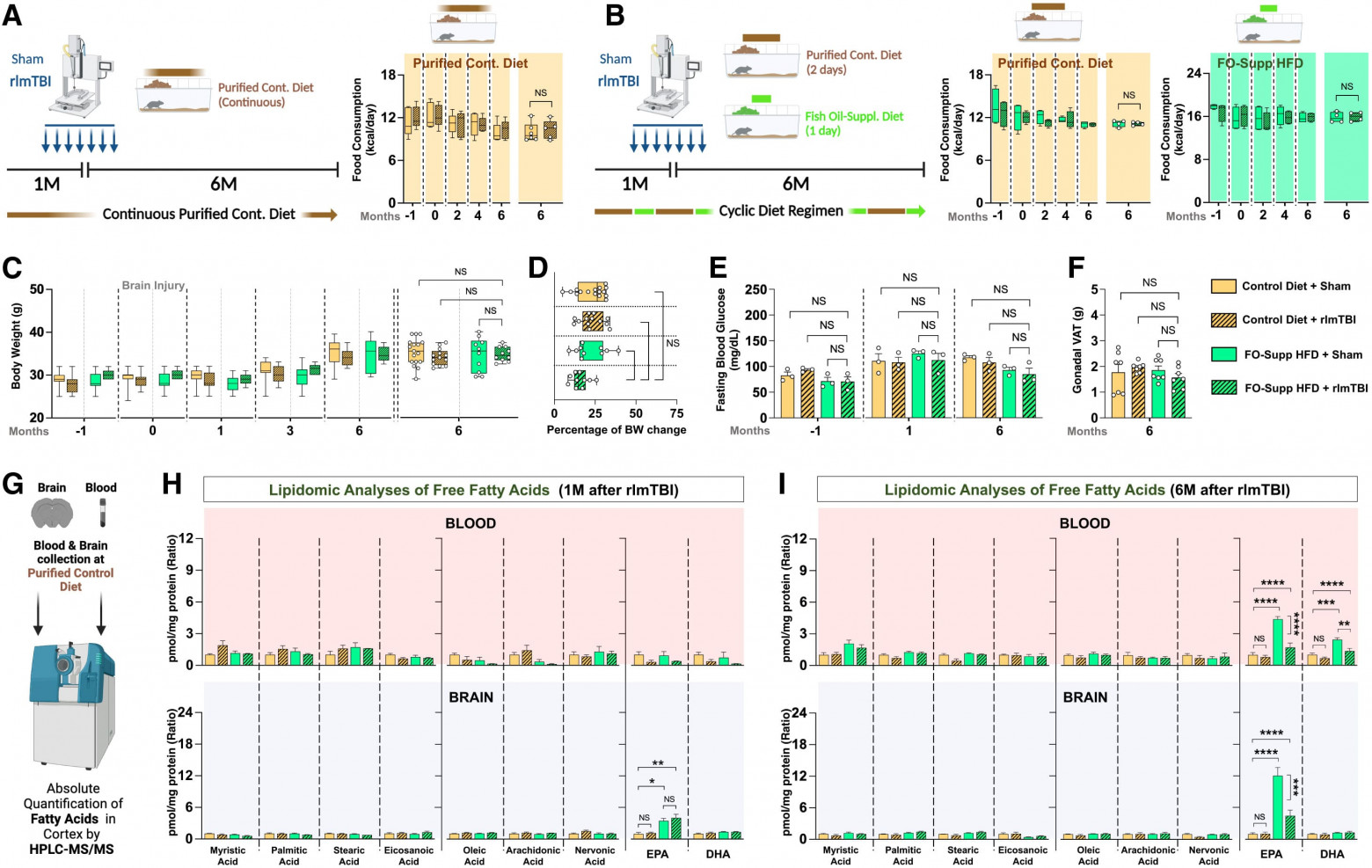
Для моделирования хронического воздействия n-3 PUFA в физиологически значимых условиях был внедрен циклический режим высокожировой диеты с добавлением рыбьего жира (FO-Suppl. HFD или FO для сокращения) у мышей дикого типа C57BL/6J, начиная с двухмесячного возраста. Эта диета чередовала один день FO с двумя днями контрольной диеты, имитируя колеблющиеся схемы приема добавок у человека. Контрольные животные содержались на непрерывной очищенной диете. После 1 месяца диеты мыши подвергались либо повторяющимся легким закрытым черепно-мозговым травмам (rlmTBI), либо фиктивным процедурам, после чего продолжалось воздействие диеты в течение дополнительных 6 месяцев для оценки хронических последствий после травмы (1A и 1B).
Важно отметить, что FO диета не влияла на общее потребление калорий, массу тела, уровень глюкозы в крови натощак или ожирение при различных условиях питания и травм (1A–1F), что подтверждает сохранение системного метаболического гомеостаза на протяжении всего исследования. Однако количественное определение неэтерифицированных (свободных) жирных кислот с помощью высокоэффективной жидкостной хроматографии-тандемной масс-спектрометрии (HPLC-MS/MS от high-performance liquid chromatography-tandem mass spectrometry) выявило поразительную липидную сигнатуру головного мозга: EPA избирательно и интенсивно накапливалась в мозге контрольных мышей, получавших циклическую диету с добавкой FO (1G и 1H), что указывает на относительную устойчивость к метаболизму полиненасыщенных жирных кислот в условиях отсутствия травм. Это накопление было специфично для EPA и не воспроизводилось DHA, что предполагает различные метаболические судьбы n-3 PUFA в головном мозге.
Примечательно, что этот резервуар не был статичным: у мышей rlmTBI уровень EPA в головном мозге заметно снижался с течением времени (1I), в то время как уровень DHA оставался неизменным. Это предполагает, что травма нарушает избирательное удержание PUFA. Через 6 месяцев после травмы у животных с черепно-мозговой травмой (rlmTBI), получавших рыбий жир, наблюдалось значительное снижение уровня EPA в головном мозге по сравнению с контрольной группой без rlmTBI, что сопровождалось снижением уровня циркулирующей EPA. Однако уровень EPA в плазме у мышей с rlmTBI, получавших рыбий жир, оставался выше, чем в контрольных группах без rlmTBI и пищевых добавок. Через шесть месяцев у мышей, получавших рыбий жир, также наблюдалось умеренное увеличение уровня циркулирующей DHA, в то время как уровень DHA в коре головного мозга оставался неизменным, что согласуется с жестко регулируемой и относительно медленной адаптацией DHA в головном мозге по сравнению с более динамично реагирующим пулом EPA. В отличие от этого, DHA оставалась удивительно стабильной как в крови, так и в головном мозге, что подтверждает точку зрения [4] о том, что EPA уникальным образом реагирует на метаболические сдвиги, вызванные травмой.
В совокупности эти результаты показывают, что, хотя длительное добавление рыбьего жира приводит к накоплению EPA в исходных условиях, уровень EPA в головном мозге снижается после черепно-мозговой травмы, что указывает на динамическое, связанное с травмой изменение удержания полиненасыщенных жирных кислот. Вместо того чтобы служить пассивным нейропротекторным резервом, EPA, по-видимому, метаболически участвует в реакции мозга на травму. Примечательно, что, хотя диета с добавлением рыбьего жира обеспечивала более высокие абсолютные уровни нескольких насыщенных и мононенасыщенных жирных кислот, эти более широкие диетические различия не привели к пропорциональным изменениям в неэтерифицированных пулах. Уровень EPA был уникально повышен как в плазме, так и в головном мозге, что подчеркивает замечательную специфичность метаболического ответа на диетическое вмешательство. На хронической стадии после травмы уровень EPA у мышей с rlmTBI, получавших рыбий жир, снижался по сравнению с группой без rlmTBI, что отражает метаболическую активность в поврежденном мозге, но оставался существенно выше, чем в контрольных группах, демонстрируя высокоизбирательную адаптацию как к потреблению пищи, так и к травме. В совокупности эти закономерности указывают на то, что доступность EPA определяется не только системным поступлением, но и отражает скоординированные, связанные с травмой изменения в усвоении EPA. Это подтверждает точку зрения о том, что EPA является наиболее динамично задействованным n-3-соединением в метаболических сдвигах, вызванных травмой.
Нейроваскулярная нестабильность, вызванная EPA, провоцирует периваскулярную таупатию и снижение когнитивных функций после rlmTBI
Повторяющиеся легкие ЧМТ (rmTBI) являются известным предшественником CTE (хронической травматической энцефалопатии), однако механизмы, посредством которых ранние нейроваскулярные нарушения способствуют долгосрочному снижению когнитивных функций, остаются недостаточно изученными. Остается неясным, отражает ли это ухудшение только кумулятивную нагрузку от травмы или возникает в результате отсроченных, дезадаптивных метаболических сдвигов, которые перестраивают цереброваскулярную функцию. Учитывая важную роль липидного метаболизма в поддержании нейроваскулярной единицы (NVU), ученые предположили, что длительное воздействие n-3 PUFA, особенно EPA, на организм может метаболически подготовить NVU, и особенно ее эндотелиальный компонент, к дисфункции после травмы.
Изображение №2
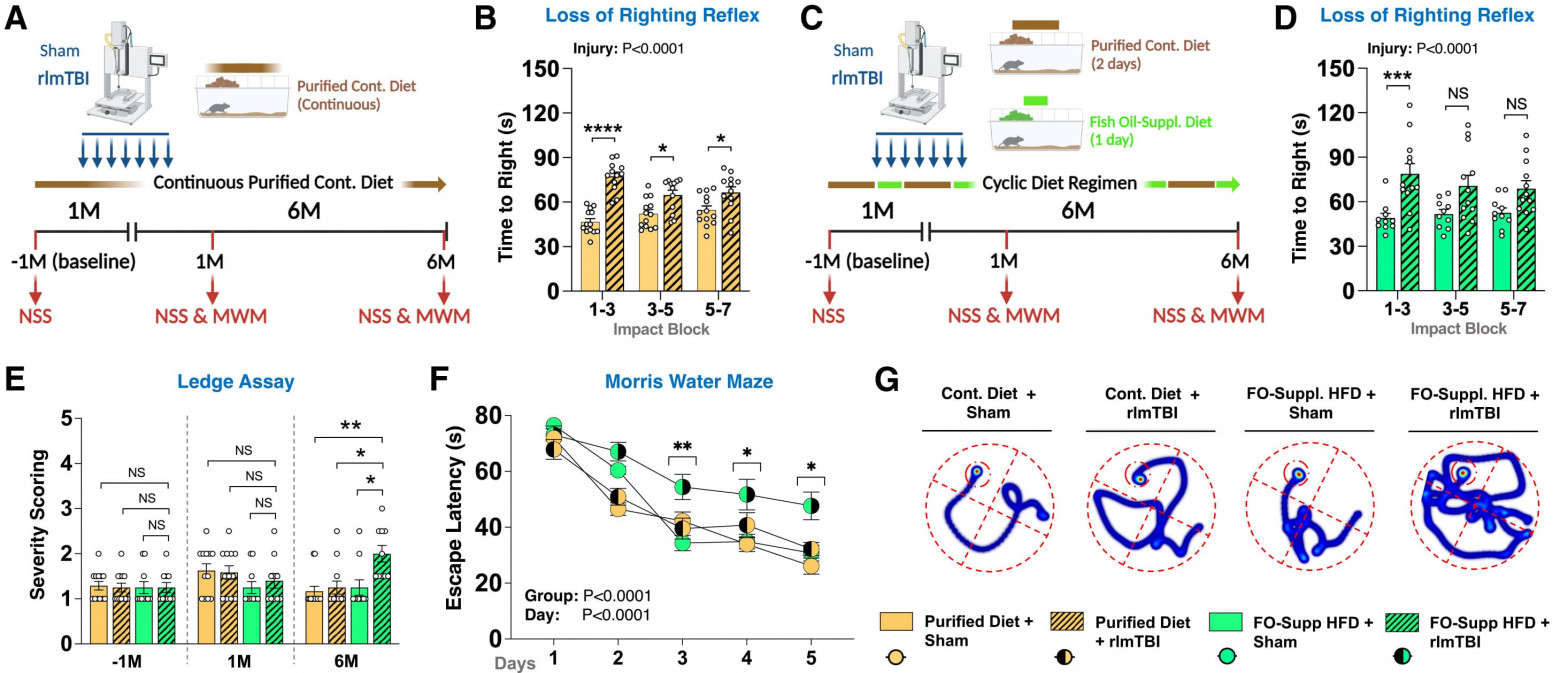
Используя разработанную учеными парадигму FO + rlmTBI, ученые далее исследовали, влияет ли диетический фон на острое неврологическое подавление, вызванное травмой. Восстановление выпрямительного рефлекса [5], стандартного показателя преходящего неврологического подавления после удара, а не постоянной потери функции, было значительно замедлено у мышей rlmTBI по сравнению с контрольной группой как в группе с контрольной диетой (2A и 2B), так и в группе с FO питанием (2C и 2D).
Важно отметить, что латентность выпрямительного рефлекса [6] не различалась между мышами rlmTBI, получавшими контрольную диету, и мышами, получавшими FO питание. Это указывает на эквивалентность начальной тяжести травмы при различных диетических условиях. Однако долгосрочные результаты различались между группами, получавшими разные диеты. У мышей, получавших контрольную диету, наблюдались стабильные неврологические показатели и сохранность пространственного обучения [7] с течением времени, без признаков хронических нарушений (2E–2G). В отличие от них, у мышей, получавших FO, развились отсроченные поведенческие отклонения, которые стали очевидны через 6 месяцев после травмы.
Двухфакторный дисперсионный анализ с повторными измерениями показателей тяжести неврологических нарушений выявил значимое взаимодействие группы и времени, а апостериорный тест Даннетта показал более высокие показатели через 6 месяцев у животных группы FO + rlmTBI по сравнению со всеми другими группами, тогда как на исходном уровне или через 1 месяц различий не было обнаружено (2E). Эффективность пространственного обучения в водном лабиринте Морриса оценивалась с использованием модели смешанных эффектов на протяжении 5-дневной фазы обучения. Этот анализ показал значительные эффекты времени и группы, а также взаимодействие времени и группы. Постхоковые сравнения Бонферрони показали, что у мышей FO + rlmTBI наблюдалось большее время побега, чем у всех других групп, в дни обучения 3–5, что указывает на нарушение пространственного обучения в условиях длительного приема FO (2F). В соответствии с нарушением обучения, тепловые карты на 5-й день продемонстрировали точное, целенаправленное плавание в контрольных группах, тогда как FO мыши продолжали полагаться на поиск по периметру, что указывает на неспособность сформировать эффективную пространственную память [8] о местоположении платформы (2G).
В совокупности эти результаты показывают, что хроническое высокожировое питание с добавлением FO выявляет отсроченную, зависящую от диеты уязвимость нейроповеденческих функций после rlmTBI, в то время как животные на контрольной диете сохраняют долговременную поведенческую устойчивость.
Изображение №3
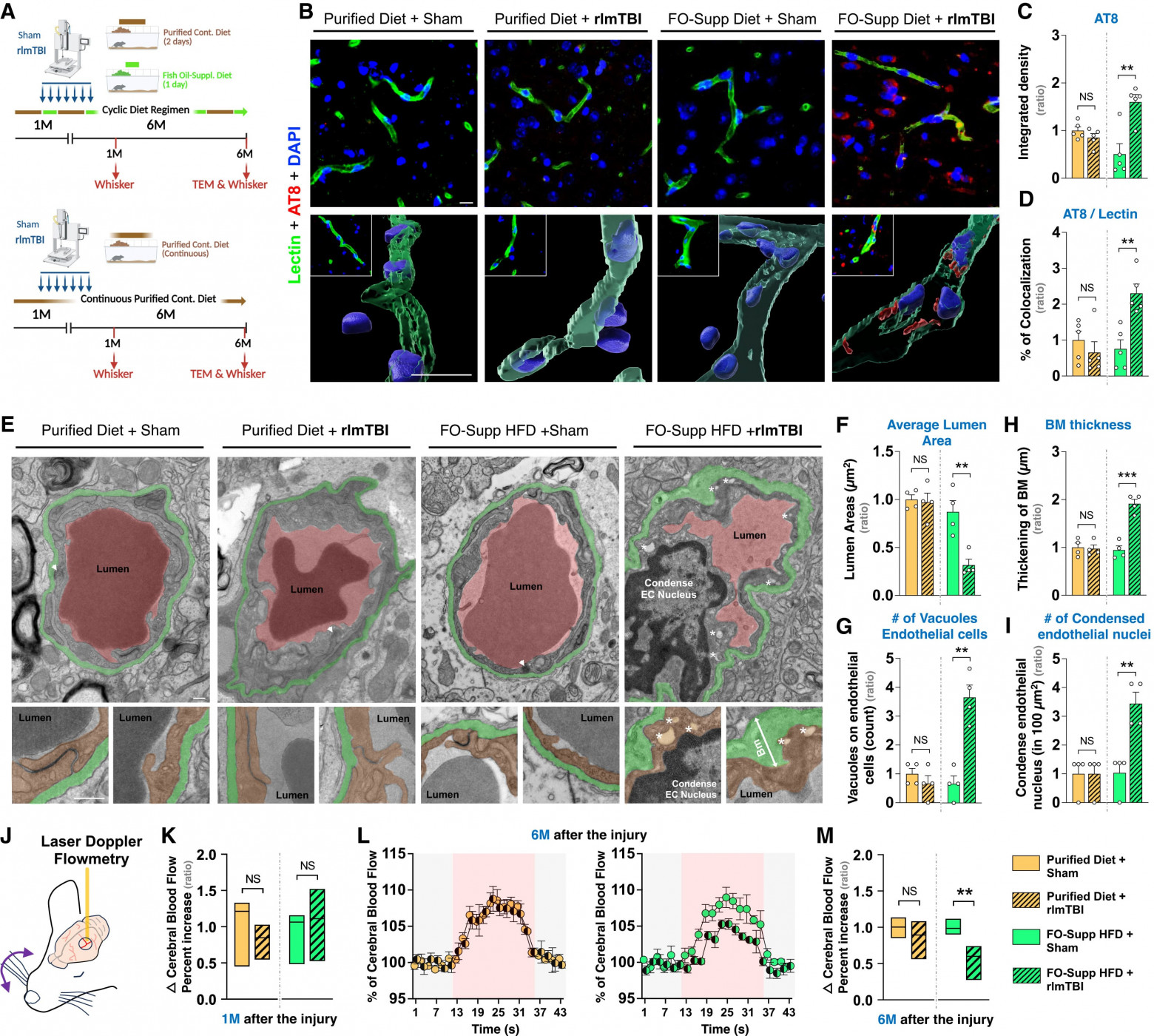
Гистопатологический анализ связал эти поведенческие нарушения с появлением периваскулярной тау-патологии, характерного признака ранней стадии CTE (3A). Иммуноокрашивание на гиперфосфорилированный тау (AT8) выявило существенное накопление как в нейронах, так и в периваскулярных компартментах поврежденной коры головного мозга у rlmTBI мышей, получавших FO (3B–3D). Примечательно, что положительный сигнал AT8 показал выраженную пространственную ассоциацию [9] с лектин-меченой микрососудистой сетью, что указывает на сосудистые компартменты как на ключевое место агрегации тау. В соответствии с этим, дополнительное коиммуноокрашивание NeuN подтвердило повышенное накопление AT8 в нейронах в тех же областях, указывая на то, что тау-патология распространяется за пределы сосудистой сети, оставаясь при этом тесно связанной с микрососудистыми доменами.
Для дальнейшего уточнения паренхимальных коррелятов замедленного снижения поведенческих функций ученые провели количественный анализ плотности нейронов, синаптической целостности и активации микроглии через 6 месяцев после травмы. У FO + rlmTBI мышей иммуноокрашивание NeuN выявило умеренное, но значительное снижение плотности нейронов по сравнению с контрольной группой. Примечательно, что эта избирательная уязвимость нейронов проявилась на фоне сохраненной плотности, интегрированной с синаптофизином, во всех группах. Это указывает на то, что содержание пресинаптических белков и синаптическая структура оставались неповрежденными, несмотря на потерю нейронов. Аналогично, иммунореактивность Iba1 не показала значительных различий, что свидетельствует об отсутствии стойкой активации микроглии на этой хронической стадии.
Для оценки структурной и функциональной целостности NVU ученые провели трансмиссионную электронную микроскопию (TEM от transmission electron microscopy) и измерили нейроваскулярную связь посредством вызванных движением вибрисс мозговых кровотоков. Через 6 месяцев после травмы у FO + rlmTBI мышей наблюдалось выраженное ремоделирование цереброваскулярной системы, включая сужение просвета сосудов (FO) и утолщение базальных мембран (3G), а также широко распространенную дегенерацию эндотелия, характеризующуюся цитоплазматической вакуолизацией (3H) и конденсацией ядра (3I).
Ядра эндотелия выглядели гиперхроматическими и конденсированными, в отличие от диффузного эухроматина у контрольных мышей, что согласуется с остановкой транскрипции и метаболическим стрессом [10] в структурно поврежденной NVU. Важно отметить, что эти ультраструктурные аномалии сопровождались функциональными нарушениями, что отражалось в ослабленной реакции мозгового кровотока на сенсорную стимуляцию (3J–3M), указывая на нарушение нейроваскулярной связи. Напротив, анализы целостности барьера, включая экстравазацию IgG и окрашивание по Прусскому синему, не выявили явной проницаемости на этом хроническом этапе.
В совокупности эти данные указывают на хронический нейроваскулярный фенотип, при котором существенная перестройка базальной мембраны и повреждение эндотелия совпадают с нарушением вызванной стимулом [11] гемодинамической регуляции, даже когда стандартные методы измерения проницаемости не выявляют явной экстравазации.
Учитывая эти структурные и функциональные изменения, далее была выполнена оценка, влияет ли хроническая FO диета на перекисное окисление липидов в головном мозге. Количественное определение 4-гидроксиноненаля (4-HNE) с помощью иммуногистохимии и вестерн-блоттинга через 6 месяцев после травмы выявило тенденцию к повышению уровня 4-HNE как в группе FO, так и в группе FO + rlmTBI по сравнению с контрольной группой, хотя эти различия не достигли статистической значимости. Это умеренное, статистически незначимое увеличение предполагает незначительное повышение перекисного окисления липидов при длительном воздействии омега-3, однако его вклад в хроническую нейроваскулярную дисфункцию еще предстоит определить.
В совокупности эти данные свидетельствуют о том, что длительное обогащение рациона EPA может влиять на нейрососудистую структуру и функцию после черепно-мозговой травмы, потенциально способствуя развитию таупатии и когнитивных нарушений с течением времени. Эта патофизиологическая последовательность, характеризующаяся дегенерацией эндотелия в нейроваскулярной единице, утолщением базальной мембраны и нарушением гемодинамических реакций, происходит без явного нарушения гематоэнцефалического барьера (BBB от blood-brain barrier), что указывает на субклиническую форму нейроваскулярной дисфункции. Эти результаты предполагают, что длительное воздействие EPA может способствовать цереброваскулярному ремоделированию и влиять на уязвимость мозга к прогрессирующему ухудшению, подчеркивая важность учета контекста при интерпретации эффектов n-3 PUFA.
EPA перепрограммирует кортикальные транскрипционные ответы и подавляет ангиогенную сигнализацию после rlmTBI
Изображение №4
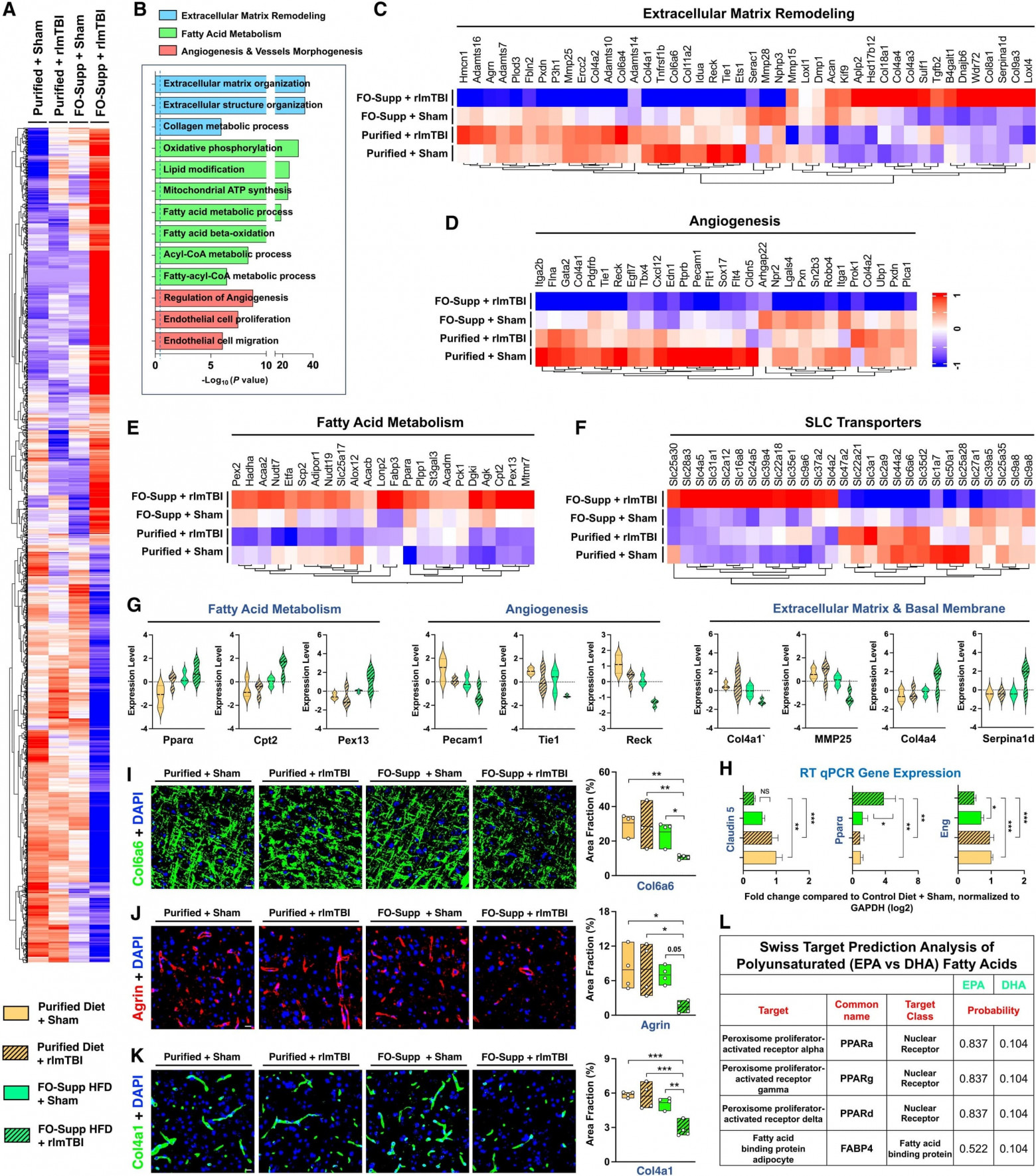
Для механистического анализа транскрипционных программ, лежащих в основе нейроваскулярной хрупкости, вызванной EPA, ученые провели секвенирование РНК [12] (RNA-seq) с последующим анализом взвешенной сети коэкспрессии генов (WGCNA от weighted gene co-expression network analysis) на поврежденной кортикальной ткани FO + rlmTBI мышей. Этот системный подход позволил идентифицировать дискретные генные модули, избирательно измененные у FO + rlmTBI мышей по сравнению со всеми контрольными группами. Среди 32057 проанализированных транскриптов иерархическая кластеризация выявила 30 собственных модулей, два из которых, MEpurple (1323 гена) и MEdarkred (743 гена), были значительно обогащены в группе FO + rlmTBI, представляя собой уникальную молекулярную сигнатуру хронического воздействия PUFA в поврежденном мозге (4A).
Анализ генной онтологии этих модулей выявил широко распространенную дисрегуляцию транскрипционных программ, критически важных для гомеостаза ECM, ангиогенной сигнализации, пролиферации и миграции эндотелиальных клеток, а также путей метаболизма липидов, включая обмен жирных ацил-КоА (4B). Тепловые карты экспрессии и скрипичные диаграммы дополнительно продемонстрировали отчетливые транскрипционные сдвиги в различных категориях, таких как ремоделирование внеклеточного матрикса, ангиогенез и метаболизм жирных кислот, наряду с нарушениями в работе транспортеров растворенных веществ (SLC от solute carrier), необходимых для обмена питательных веществ в эндотелии головного мозга (4C–4G). В совокупности эти данные свидетельствуют о том, что хроническое воздействие FO после rlmTBI вызывает скоординированное изменение механизмов нейроваскулярного восстановления и метаболической адаптации. У FO + rlmTBI животных наблюдалось выраженное подавление генов, необходимых для структурной целостности внеклеточного матрикса и стабильности сосудов.
Критические компоненты внеклеточного матрикса, такие как Agrn, Tie1 и Reck, ключевые регуляторы синаптического закрепления, сосудистого гомеостаза и ингибирования матриксных металлопротеиназ (MMP от matrix metalloproteinase), были значительно подавлены. Также были подавлены множественные гены α-коллагена, необходимые для формирования базальной мембраны (Col4a1, Col4a2, Col6a4, Col6a6 и Col11a2), наряду с регуляторами обновления внеклеточного матрикса из семейства протеаз Adamts (Adamts7, Adamts10, Adamts14 и Adamts16), что указывает на нарушение способности к ремоделированию сосудов. Напротив, наблюдалось повышение экспрессии профибротических генов и генов, участвующих в отложении внеклеточного матрикса, включая Tgfb2 и Serpina1d, а также фибротических изоформ коллагена (Col18a1, Col4a3, Col4a4, Col8a1 и Col9a3), что указывает на неадекватное ремоделирование внеклеточного матрикса и чрезмерное его накопление.
Ключевые регуляторы ангиогенеза и стабильности эндотелия также были в значительной степени подавлены. Экспрессия Cldn5, Pecam1, Itga1 и Itga2b, генов, связанных с эндотелиальными соединениями и адгезией, была значительно снижена в группе FO + rlmTBI. Кроме того, компоненты проангиогенной сигнализации, включая Pdgfrβ, Cxcl12 и компоненты сосудистой базальной мембраны Col4a1/Col4a2, были значительно снижены, что отражает ослабленный ангиогенный ответ в головном мозге группы FO + rlmTBI. Интересно, что классические проангиогенные лиганды, такие как VEGFA, Angpt1/2 и FGF2, не были значительно изменены. Вместо этого изменения были обогащены структурными, матриксными и цитоскелетными генами, что позволяет предположить, что EPA нарушает ангиогенную активность посредством дестабилизации эндотелия, а не прямого ингибирования ангиогенных сигнальных каскадов.
Одновременно транскриптомный анализ выявил сдвиг в сторону усиления липидного метаболизма. Гены, участвующие в поглощении жирных кислот и внутриклеточной обработке, включая Ppara, Fabp3, Cpt2, Acaa2, Pex2 и Pex13, были значительно активированы в поврежденной коре головного мозга мышей, получавших диету с высоким содержанием жиров и добавок FO. Поскольку эти данные получены из общей ткани коры головного мозга, эти гены нельзя отнести к одному типу клеток, и многие из них экспрессируются множеством нервных и сосудистых клеток. Однако все больше данных свидетельствует о том, что эндотелиальные клетки используют жирные кислоты для гомеостаза и ангиогенеза, и что белки, связывающие жирные кислоты, участвуют в функции эндотелия. Это предполагает, что изменения в путях обработки липидов могут влиять как на сосудистое, так и на паренхимальное метаболическое состояние после травмы.
Соответственно, скоординированная активация этих генов согласуется с более широким кортикальным метаболическим перепрограммированием, которое способствует задействованию жирных кислот, потенциально с участием нейроваскулярного компартмента. Вместо поддержки репаративного биосинтеза этот сдвиг может отражать неадаптивное перераспределение метаболических ресурсов в посттравматической среде. Параллельные транскриптомные изменения также наблюдались в генах транспортеров SLC, включая Slc22a18, Slc28a3, Slc16a8 и Slc1a7, которые регулируют поток ионов, питательных веществ и метаболитов через BBB. Нарушение этих транспортных систем может еще больше ухудшить сосудистый и метаболический гомеостаз после травмы. Для подтверждения этих транскриптомных тенденций было проведено иммунофлуоресцентное окрашивание поврежденных кортикальных срезов, которое подтвердило снижение экспрессии белков, связанных с внеклеточным матриксом, Col6a6, Agrn и Col4a1 (4I–4K). Количественный анализ обратной транскрипции PCR (RT-qPCR) дополнительно подтвердил нарушение транскрипции, выявив снижение экспрессии маркеров стабильности эндотелия — клаудина-5 и эндоглина (Eng) — наряду с повышением экспрессии Ppara (4H), что согласуется с вызванным FO ремоделированием эндотелия в поврежденном мозге.
Липидомический анализ в течение 6 месяцев выявил устойчивое накопление EPA в головном мозге у животных, получавших диету с высоким содержанием жиров и добавок FO, но без rlmTBI. Однако после травмы уровень EPA избирательно и существенно снижался у мышей с rlmTBI, несмотря на продолжающееся диетическое воздействие, что указывает на преимущественную мобилизацию и метаболическое использование EPA в условиях повышенной потребности [13] в энергии. В отличие от этого, уровень DHA оставался неизменным, что подчеркивает избирательную уязвимость в метаболизме EPA. Это снижение, последовавшее за предварительным обогащением EPA, может отражать эффект метаболической подготовки, влияющий на транскрипционные ответы после травмы. Для дальнейшего выяснения механизма, лежащего в основе избирательности EPA, было проведено in silico прогнозирование мишеней с использованием SwissTargetPrediction. Этот анализ выявил высокие прогнозируемые вероятности связывания EPA с ядерными рецепторами [14], включая рецепторы, активируемые пролифераторами пероксисом (PPAR от peroxisome proliferator-activated receptor), и белки, связывающие жирные кислоты, такие как FABP4 (4L).
Эти результаты позволяют предположить, что EPA, но не DHA, может преимущественно взаимодействовать с транскрипционными регуляторами метаболизма жирных кислот, что согласуется с транскриптомными данными, указывающими на модуляцию генных сетей, реагирующих на жирные кислоты и участвующих в сосудистой и метаболической адаптации к повреждению.
В совокупности эти результаты показывают, что длительное воздействие EPA с пищей в контексте травмы головного мозга вызывает скоординированный транскриптомный сдвиг, характеризующийся нарушением организации внеклеточного матрикса, подавлением ангиогенной и репаративной сигнализации, усилением путей окисления жирных кислот и нарушением регуляции транспортных систем гематоэнцефалического барьера. Эта молекулярная перестройка может отражать снижение метаболической гибкости и изменение нейроваскулярного гомеостаза в контексте посттравматического стресса [15]. Устанавливая механистическую связь между накоплением EPA, вызванным травмой метаболическим перепрограммированием и неудачным восстановлением, эти результаты ставят под сомнение давние предположения о пользе n-3 PUFA и выявляют скрытый риск в липидных вмешательствах.
Использование EPA в благоприятных метаболических условиях нарушает ангиогенез и целостность эндотелия, воспроизводя цереброваскулярную дисфункцию после ЧМТ
Ангиогенез является краеугольным камнем нейроваскулярного восстановления после TBI, требуя скоординированного взаимодействия между эндотелиальными клетками, ремоделированием внеклеточного матрикса и адаптивным энергетическим метаболизмом. В исследуемой модели in vivo длительное воздействие циклической диеты с добавкой FO-Suppl. HFD привело к прогрессивному накоплению EPA в головном мозге в гомеостатических условиях; однако после TBI уровни EPA избирательно снижались, что указывает на преимущественную мобилизацию во время фазы восстановления и предполагает участие EPA в устойчивом, связанном с травмой липидном ремоделировании. Этот сдвиг сопровождался выраженными транскриптомными признаками подавления ангиогенеза, дестабилизации внеклеточного матрикса и перепрограммирования липидного метаболизма. Это предполагает, что воздействие EPA может предрасполагать сосудистую систему к неадаптивному ремоделированию и ухудшать восстановление после травмы.
Для механистического исследования этой уязвимости ученые использовали эндотелиальные клетки микрососудов костного мозга (BMVEC от brain microvessel endothelial cells), основные клеточные медиаторы ангиогенеза и стабильности сосудов, чтобы оценить, оказывает ли EPA прямое воздействие на репаративные процессы в условиях, благоприятствующих взаимодействию жирных кислот, тем самым имитируя метаболическую среду после черепно-мозговой травмы. В физиологических условиях BMVEC преимущественно используют гликолиз для производства ATP (АТФ или аденозинтрифосфат), что отражает присущее им метаболическое предпочтение глюкозы перед жирными кислотами из-за их ограниченной способности к β-окислению. Однако после травмы повышенные энергетические потребности могут вызвать компенсаторный сдвиг в метаболизме эндотелия, приводящий к увеличению зависимости от альтернативных субстратов, таких как жирные кислоты. Для моделирования этого сдвига in vitro была создана благоприятная метаболическая среда в клетках BMVEC человека (HBEC-5i) с помощью AICAR, агониста AMP-активированной протеинкиназы (AMPK), который повышает гибкость митохондриальных субстратов, и L-карнитина, кофактора, облегчающего транспорт длинноцепочечных жирных кислот в митохондрии. Этот подход имитирует условия после травмы, благоприятствующие взаимодействию жирных кислот, и позволяет целенаправленно исследовать влияние EPA и DHA на цереброваскулярную адаптацию.
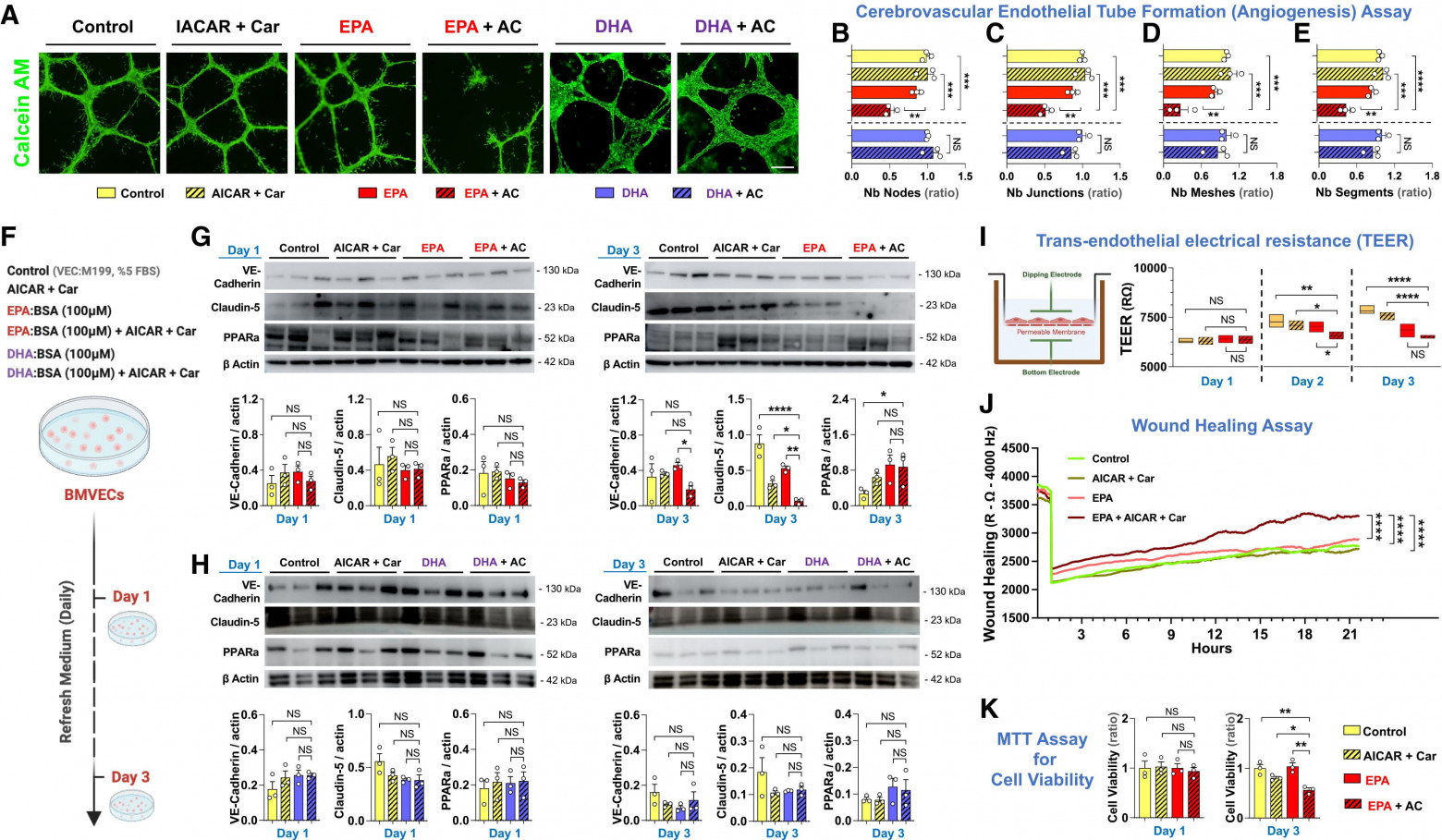
Изображение №5
EPA, но не DHA, была связана со снижением формирования ангиогенной сети в условиях, благоприятствующих образованию жирных кислот. В эксперименте по формированию эндотелиальных трубок EPA (100 мкМ) в сочетании с AICAR и L-карнитином (EPA + AC) значительно нарушала формирование сосудистой сети, уменьшая количество узлов (5B), соединений (5C), сегментов (5D) и сетчатых структур (5E) по сравнению с контрольной группой и группой, получавшей только EPA. В отличие от этого, DHA (100 мкМ) с AICAR-карнитином или без него не оказывала существенного влияния на ангиогенную способность (5A–5E). Это предполагает, что EPA может препятствовать формированию ангиогенной сети в метаболических условиях, усиливающих использование жирных кислот, и подчеркивает повышенную чувствительность эндотелия к воздействию EPA в таких условиях.
Концентрации EPA и DHA in vitro (100 мкМ) были выбраны таким образом, чтобы отражать верхние пределы воздействия, достижимые при многократном добавлении или накоплении в микродоменах. Важно отметить, что EPA сама по себе не влияла на ангиогенез в стандартной культуре, но нарушала репаративную динамику только при благоприятной метаболической стимуляции, что подчеркивает контекстно-зависимый механизм. Для исследования молекулярных основ этой дисфункции ученые оценили экспрессию клаудина-5 и VE-кадгерина, ключевых структурных белков, необходимых для эндотелиальной когезии, наряду с липид-чувствительным ядерным рецептором PPARα. Обработка EPA в условиях, благоприятствующих воздействию жирных кислот (EPA + AC), но не DHA, вызывала прогрессирующее снижение экспрессии как клаудина-5, так и VE-кадгерина, сопровождающееся повышением экспрессии PPARα (5F–5H). Эти результаты свидетельствуют о том, что воздействие EPA в условиях, благоприятствующих воздействию жирных кислот, может влиять на эндотелиальный фенотип и снижать ангиогенную способность.
Для оценки функциональных последствий измерения импеданса в реальном времени с использованием метода электрохимического импедансного зондирования клеточной подложки (ECIS от electric cell-substrate impedance sensing) выявили быстрое снижение трансэндотелиального электрического сопротивления (TEER от trans-endothelial electrical resistance) в течение 48 часов после обработки EPA + AC, которое продолжало ухудшаться до 3-го дня (5I). Это указывает на нарушение целостности монослоя и подавление его расширения. В дополнительном анализе заживления ран на основе ECIS, EPA + AC значительно замедлили закрытие эндотелиальной раны, в то время как EPA сама по себе не оказала заметного эффекта (5J). Анализы с использованием 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромида (MTT) дополнительно подтвердили эти результаты, показав зависимое от времени снижение жизнеспособности BMVEC в условиях EPA + AC (5K).
Эти результаты показывают, что EPA, будучи метаболически активированной в условиях, благоприятствующих увеличению потока жирных кислот, нарушает ангиогенную сигнализацию, дестабилизирует эндотелиальную когезию и ухудшает репаративную способность, воспроизводя ключевые эндотелиальные особенности нейроваскулярной дисфункции, наблюдаемой in vivo после длительного воздействия высококалорийной диеты с добавлением FO при черепно-мозговой травме легкой степени.
Мозг при CTE демонстрирует нейроваскулярную и жирнокислотную метаболическую перестройку, соответствующую уязвимости, связанной с EPA
CTE — это прогрессирующее нейродегенеративное заболевание, связанное с повторяющимися травмами головы, но роль хронической метаболической дисфункции, особенно в обработке жирных кислот, остается невыясненной. Все больше данных свидетельствует о том, что помимо прямой механической травмы, метаболическая негибкость может способствовать цереброваскулярной уязвимости. Хотя исследуемые модели in vivo и in vitro демонстрируют, что EPA избирательно мобилизуется при вызванной травмой метаболической потребности, дестабилизируя архитектуру эндотелия и нарушая репаративную сигнализацию, остается неясным, характеризуется ли хроническое состояние заболевания сходными или различными формами дисрегуляции PUFA. Для решения этой проблемы ученые исследовали посмертные образцы ткани головного мозга от нейропатологически подтвержденных случаев CTE, стремясь определить, сохраняются ли признаки неадаптивного метаболизма жирных кислот и цереброваскулярной дисфункции в хронической фазе заболевания. Этот анализ на людях обеспечивает трансляционный контекст для интерпретации наших экспериментальных результатов и расширяет их значимость для клинической нейродегенерации.
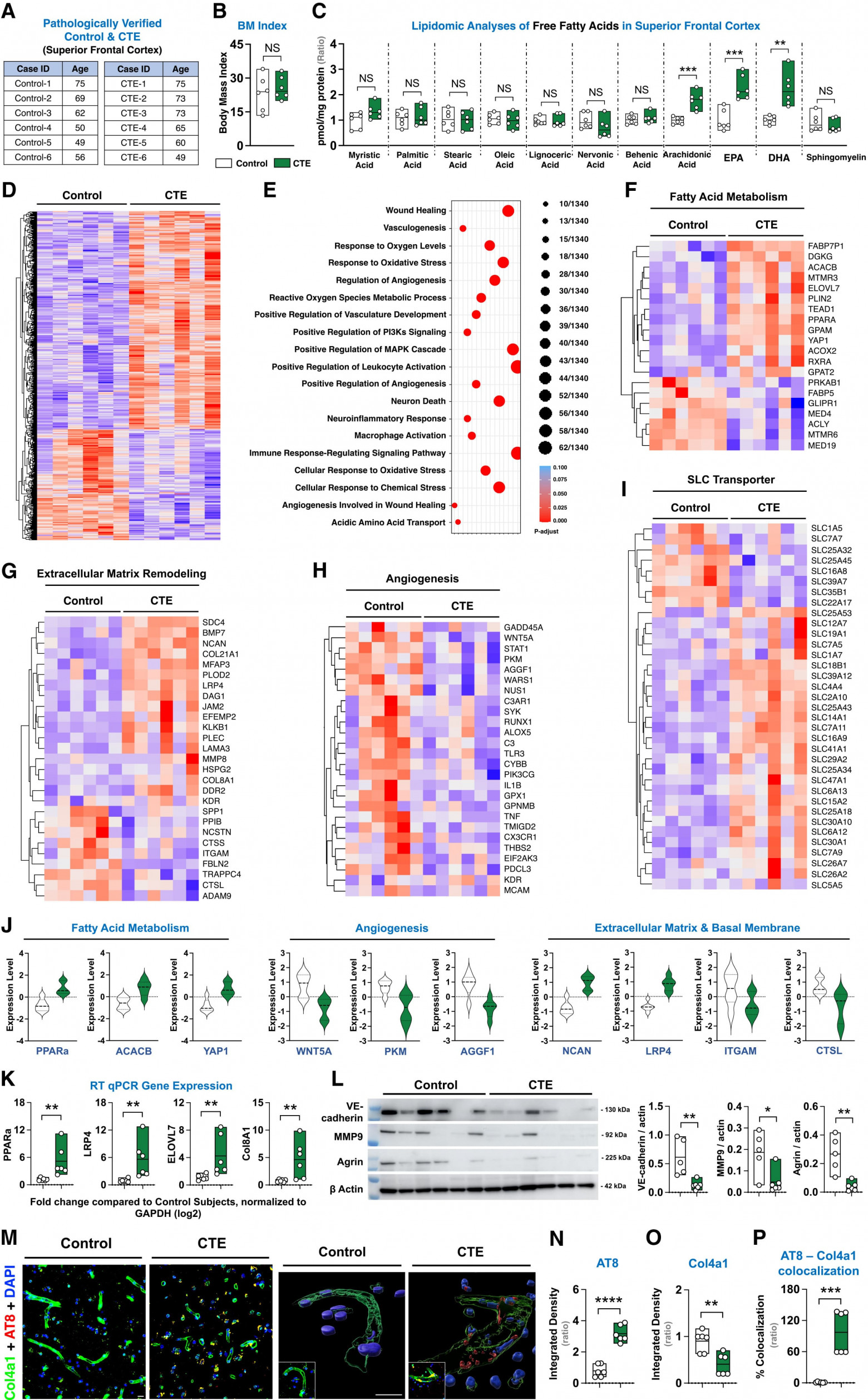
Изображение №6
Ученые проанализировали ткань верхней лобной коры головного мозга шести пациентов с подтвержденным нейропатологическим диагнозом CTE, имевших в анамнезе повторяющиеся черепно-мозговые травмы (все младше 75 лет), и шести контрольных лиц, соответствующих по возрасту и полу, с нормальным неврологическим статусом (6A). Липидомический анализ с помощью HPLC-MS/MS выявил значительное обогащение полиненасыщенными жирными кислотами (PUFA) в головном мозге пациентов с CTE, включая повышение содержания EPA и DHA примерно на 150% и увеличение содержания арахидоновой кислоты (AA от arachidonic acid) на 80% по сравнению с контрольной группой (6C). Важно отметить, что эти различия не зависели от индекса массы тела (6B), что указывает на внутренние, специфичные для головного мозга, изменения в метаболизме жирных кислот.
Это регионально-специфическое накопление PUFA может отражать метаболическое нарушение, контрастирующее с истощением EPA, наблюдаемым в мышиной модели, — однако оба паттерна указывают на нарушение гомеостатического метаболизма PUFA в контексте травматического стресса. Чтобы определить, сопровождалось ли это метаболическое нарушение более широкой транскрипционной перестройкой, ученые провели секвенирование РНК на парных образцах кортикальной ткани от подтвержденных случаев CTE и контрольной группы. Анализ дифференциальной экспрессии выявил 2678 значительно нарушенных генов (6D), охватывающих ключевые биологические области, включая метаболизм жирных кислот, ремоделирование внеклеточного матрикса, ангиогенез и нейровоспаление (6E). Пути метаболизма жирных кислот продемонстрировали широко распространенные нарушения (6F), включая дифференциальную регуляцию генов, управляющих окислением (например, PRKAB1 и ACACB), элонгацией (например, ELOVL7) и десатурацией.
Снижение экспрессии FABP5, ACLY и MTMR6 указывает на нарушение липидного обмена и снижение способности к энергетическому распознаванию, тогда как повышение экспрессии PPARA, YAP1, TEAD1 и PLIN2 указывает на усиление пероксисомального липидного обмена и образования липидных капель, что является признаками метаболической перестройки. Одновременно с этим, гены, связанные с ECM (6G), были значительно изменены, включая снижение экспрессии AGRN и MMP9, критически важных для ремоделирования матрикса и синаптической стабильности, и повышение экспрессии COL8A1 и LRP4, что указывает на патологическую реструктуризацию ECM.
Транскрипты, связанные с ангиогенезом, включая VE-кадгерин (CDH5; 6H), были значительно снижены, что указывает на нарушение целостности эндотелия. Нарушения в экспрессии транспортеров растворенных веществ (SLC; 6I) указывают на дальнейшее нарушение обмена питательных веществ и ионов на границе кровь-мозг. Визуализация с помощью тепловых карт и скрипичных диаграмм (6J) выявила последовательные направленные сдвиги в ключевых кластерах генов, связанных с переработкой жирных кислот, поддержанием сосудистой системы и структурной стабильностью. qPCR (6K) и вестерн-блоттинг (6L) подтвердили дифференциальную экспрессию репрезентативных мишеней, включая PPARA, ELOVL7, LRP4, COL8A1 и VE-кадгерин.
Эти результаты согласуются с предположением, что хроническое накопление PUFA при CTE может быть связано с транскрипционным ремоделированием, влияющим на сосудистые и метаболические пути. В подтверждение стойкого нейроваскулярного нарушения иммуноокрашивание AT8 выявило накопление гиперфосфорилированного тау-белка как в нейрональных, так и в периваскулярных компартментах пораженных кортикальных областей (6M–6P), что является определяющей особенностью прогрессирования заболевания и пространственной сигнатурой, указывающей на поражение нейроваскулярной единицы. Эта картина согласуется с моделью, в которой стойкие сосудистые изменения могут быть вовлечены в прогрессирование тау-патологии при CTE.
Скоординированное нарушение метаболизма жирных кислот, ангиогенной сигнализации и ремоделирования внеклеточного матрикса определяет дезадаптивную ось, в которой нарушение метаболизма полиненасыщенных жирных кислот (PUFA) ухудшает восстановление сосудов, дестабилизирует нейроваскулярную единицу и способствует прогрессирующей нейродегенерации. Хотя остается неясным, инициируют ли эти изменения заболевание или представляют собой адаптацию к кумулятивной травме, их воспроизводимость в системах in vivo, in vitro и у человека подчеркивает общую и потенциально поддающуюся воздействию уязвимость. Эти данные позволяют предположить, что целенаправленная модуляция метаболизма PUFA в головном мозге может способствовать разработке терапевтических стратегий при черепно-мозговой травме и связанных с ней нейродегенеративных заболеваниях.
Для более детального ознакомления с нюансами исследования рекомендую заглянуть в доклад ученых [16] и дополнительные материалы [17] к нему.
Эпилог
В рассмотренном нами сегодня труде ученые рассказали о своей исследовании, которое может изменить наше мнение касательно полезности рыбьего жира, по крайней мере в определенных обстоятельствах.
Популярность различных пищевых добавок в наши дни весьма высока, несмотря на развитость фармацевтики и традиционной медицины. Как правило, пищевые добавки несут исключительно пользу, если их употребление нормировано и не выходит за пределы разумного. Однако далеко не все аспекты этих добавок известны и понятны не только потребителям, но и ученым, что делает потенциальными источниками риска для здоровья.
Первое, что отметили ученые, это различность в механизмах действия разных жирных кислот. Докозагексаеновая кислота (DHA) хорошо известна своей благотворной ролью в мозге и является важной частью нейронных мембран. Эйкозапентаеновая кислота (EPA), однако, действует по другому пути. Она в меньшей степени включается в структуры мозга, а ее эффекты могут варьироваться в зависимости от продолжительности ее воздействия и от окружающих биологических условий. Из-за этого долгосрочное влияние потребления омега-3 на восстановление мозга и адаптацию кровеносных сосудов оставалось неясным.
Для лучшего понимания этих эффектов ученые использовали ряд моделей, чтобы связать диету, функцию мозга и заживление. На мышах исследователи изучали, как длительное употребление рыбьего жира влияет на реакцию мозга на повторные легкие ЧМТ. Основное внимание уделялось сигналам, связанным со стабильностью и восстановлением кровеносных сосудов. Они также исследовали эндотелиальные клетки микрососудов головного мозга человека, которые образуют часть барьера между мозгом и кровотоком. В этих клетках EPA, но не ДГК, была связана со снижением способности к восстановлению, что согласуется с результатами, полученными на животных моделях. Дополнительно ученые использовали полученные данные для сопоставления с реальными заболеваниями мозга человека, в частности с хронической травматической энцефалопатией (CTE).
В ходе исследований было установлено, что у мышей после ЧМТ диета с добавлением рыбьего жира вызывала ухудшение неврологических показателей и пространственного обучения, а также явные признаки накопления тау-белка, связанного с сосудами, в коре головного мозга, что связывает нарушение восстановления с нейроваскулярной дисфункцией и периваскулярной тау-патологией.
В поврежденной коре головного мозга наблюдался скоординированный сдвиг в генных программах, которые обычно поддерживают стабильность и восстановление сосудов. Закономерность включала снижение экспрессии генов, связанных с организацией внеклеточного матрикса и целостностью эндотелия, наряду с более широкими изменениями, соответствующими изменению липидного обмена после травмы.
Использование EPA в благоприятных метаболических условиях нарушает ангиогенез и целостность эндотелия, воспроизводя цереброваскулярную дисфункцию при посттравматическом повреждении головного мозга. В эндотелиальных клетках микрососудов головного мозга человека EPA не действовала как универсальный токсин. Вместо этого, когда клетки помещали в условия, способствующие взаимодействию жирных кислот, EPA была связана с более слабым формированием ангиогенной сети и снижением целостности эндотелиального барьера, что соответствует ключевым особенностям дефицита нейроваскулярного восстановления, наблюдаемого in vivo.
В посмертной коре головного мозга пациентов с CTE, подтвержденной нейропатологически, и историей повторяющихся травм головного мозга ученые обнаружили признаки нарушения баланса жирных кислот и обширных транскрипционных изменений, затрагивающих сосудистые и метаболические пути.
Естественно, ученые не утверждают, что рыбий жир является исключительно вредным. Его полезные свойства нельзя исключать. Данное исследование лишь подчеркивает важность проведения более детальных анализов тех или иных пищевых добавок, а также информирование общественности о потенциальных рисках, связанных с их употреблением.
В будущем ученые планируют продолжить исследование того, как EPA перемещается по организму, включая процессы ее абсорбции, транспортировки и распределения. Особый интерес представляют механизмы, контролирующие перемещение жирных кислот.
Немного рекламы
Спасибо, что остаетесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас, оформив заказ или порекомендовав знакомым, облачные VPS для разработчиков от $4.99 [18], уникальный аналог entry-level серверов, который был придуман нами для Вас: Вся правда о VPS (KVM) E5-2697 v3 (6 Cores) 10GB DDR4 480GB SSD 1Gbps от $19 или как правильно делить сервер? [19] (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
Dell R730xd в 2 раза дешевле в дата-центре Maincubes Tier IV в Амстердаме? Только у нас 2 х Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 ТВ от $199 в Нидерландах! Dell R420 – 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB – от $99! [20] Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки? [21]
Автор: Dmytro_Kikot
Источник [22]
Сайт-источник BrainTools: https://www.braintools.ru
Путь до страницы источника: https://www.braintools.ru/article/29682
URLs in this post:
[1] кислорода: http://www.braintools.ru/article/5138
[2] реакции: http://www.braintools.ru/article/1549
[3] астроциты: http://www.braintools.ru/article/9161
[4] зрения: http://www.braintools.ru/article/6238
[5] рефлекса: http://www.braintools.ru/article/9352
[6] рефлекса: http://www.braintools.ru/article/8998
[7] обучения: http://www.braintools.ru/article/5125
[8] память: http://www.braintools.ru/article/4140
[9] ассоциацию: http://www.braintools.ru/article/621
[10] стрессом: http://www.braintools.ru/article/9548
[11] стимулом: http://www.braintools.ru/article/5596
[12] РНК: http://www.braintools.ru/article/8114
[13] потребности: http://www.braintools.ru/article/9534
[14] рецепторами: http://www.braintools.ru/article/9580
[15] стресса: http://www.braintools.ru/article/9041
[16] доклад ученых: https://www.cell.com/action/showPdf?pii=S2211-1247%2826%2900213-5
[17] дополнительные материалы: https://www.cell.com/cms/10.1016/j.celrep.2026.117135/attachment/8aa09b1b-744b-44ad-8a5a-e44936839425/mmc1.pdf
[18] облачные VPS для разработчиков от $4.99: https://ua-hosting.company/servers/vps/
[19] Вся правда о VPS (KVM) E5-2697 v3 (6 Cores) 10GB DDR4 480GB SSD 1Gbps от $19 или как правильно делить сервер?: https://habr.com/company/ua-hosting/blog/347386/
[20] 2 х Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 ТВ от $199 в Нидерландах! Dell R420 – 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB – от $99!: https://ua-hosting.company/servers/dedicated/
[21] Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?: https://habr.com/company/ua-hosting/blog/329618/
[22] Источник: https://habr.com/ru/companies/ua-hosting/articles/1029988/?utm_source=habrahabr&utm_medium=rss&utm_campaign=1029988
Нажмите здесь для печати.