«Есть великолепие в этом взгляде на жизнь, с её несколькими силами, изначально вдохнутую в несколько форм или одну; и что, в то время как эта планета движется, вращаясь в соответствии с неизменным законом гравитации, из столь простого начала развивались и развиваются бесконечные формы, самые прекрасные и самые удивительные» (Чарльз Дарвин)
«Теория эволюции Дарвина путём естественного отбора – единственное работоспособное объяснение, когда-либо предложенное для замечательного факта нашего собственного существования, да и существования всей жизни, где бы она ни появилась во Вселенной» (Джон Мейнард Смит)
«Цепь жизни непрерывна, от минералов на одном конце до самых сложных организмов на другом» (Стефан Ледук)
«Жизнь в своём развитии никогда не пренебрегала тем, что уже построено, а строила поверх того, что есть. Поэтому клетка напоминает участок археологических раскопок, где обнажается напластование одного слоя на другой – чем старше, тем глубже» (Альберт Сент-Дьёрдьи)
В первой части этой статьи мы рассмотрели две теории, дающие ключ к пониманию механизмов абиогенеза: конструкторскую теорию жизни Кьяры Марлетто и теорию диссипативной адаптации Джереми Ингланда. Одна из них объясняет, как возможны репликация, самовоспроизводство и дарвиновская эволюция без «тонко настроенных» на появление жизни законов физики, а вторая показывает, что при определённых условиях неравновесные термодинамические процессы делают самоорганизацию и жизнь более вероятными, чем их отсутствие. Но это слишком абстрактные модели, объясняющие существование не только биологической жизни в известной нам форме, но и вообще любых самовоспроизводящихся машин. А каковы практические достижения науки в деле искусственного создания жизни в лаборатории? Насколько мы близки к пониманию химического механизма получения устойчивого репликатора? Как появился генетический код и система производства белков? Существует только один способ создания жизни, или их много?
Тема сложная, а я не биохимик, чтобы рассматривать абиогенез в мельчайших деталях. Но вам, надеюсь, такие детали не нужны, а кому нужны, уже давно всё узнали из книг Михаила Никитина «Происхождение жизни. От туманности до клетки» и Александра Маркова «Рождение сложности». Поэтому я ограничусь схематическим нарративом: перечислением основных этапов абиогенеза, необходимых для этого компонентов, условий среды и химических процессов. Заодно опровергнем ещё несколько креационистских мифов и составим портрет нашего последнего универсального предка. Появление фотосинтеза, эукариотов, полового размножения, многоклеточности и других признаков сложных организмов нас сейчас не интересует – мы выясняем, как возникла простейшая бактериальная форма жизни.
Отправная точка: кем был общий предок всего живого?
Для начала вспомним определение, которое мы давали в статье «Как определить жизнь?». В самом широком значении термина жизнь – это просто самовоспроизведение с изменениями. Более точно её можно определить как активность репликатора, побуждающая окружающую среду его копировать, или, по Дэвиду Дойчу, как реализованное знание, заставляющее среду сохранять существование этого знания. Чтобы жизнь была возможна, требуется конструктор, выполняющий задачу самовоспроизводства с высокой точностью. В первой части этой статьи мы выяснили, что такой организм должен состоять из копировального аппарата, собственно конструктора и кодированного описания этих автоматов. В принципе универсальный конструктор способен сам скопировать любое описание, но в таком случае описание было бы длиннее самого конструктора, поэтому необходим отдельный копировщик. В случае биологической жизни носителями генетического кода являются нуклеиновые кислоты (ДНК и РНК), копировщиком – белковые ферменты (ДНК- и РНК-полимеразы), а конструктором – рибосома. Это минимальный набор деталей, из которых должен состоять живой организм.
Как правило, учёные выделяют три компонента жизни: генетический, метаболический и изоляционный. Генетический компонент – это способность хранить, использовать и воспроизводить информацию, которая управляет жизненными функциями. Метаболический компонент – это способность извлекать, хранить и использовать химическую энергию, необходимую для реализации жизненных функций. Изоляционный компонент – это прежде всего наличие мембраны, отделяющей генетические и метаболические механизмы клетки от окружающей среды и сохраняющей целостность организма. Гипотезы происхождения жизни также делят на генетические, ставящие на первое место появление самовоспроизводящихся молекул и молекулярный дарвинизм, метаболические, рассматривающие жизнь как результат самоорганизации диссипативных структур в условиях термодинамического неравновесия, и изоляционные, считающие важнейшим условием существования жизни концентрацию веществ и компартментализацию (разделение) биохимических реакций внутри микрокапель воды, ограниченных мембраной. Мы до сих пор точно не знаем, что возникло первым: репликатор, метаболизм или мембрана. Скорее всего, они эволюционировали параллельно.
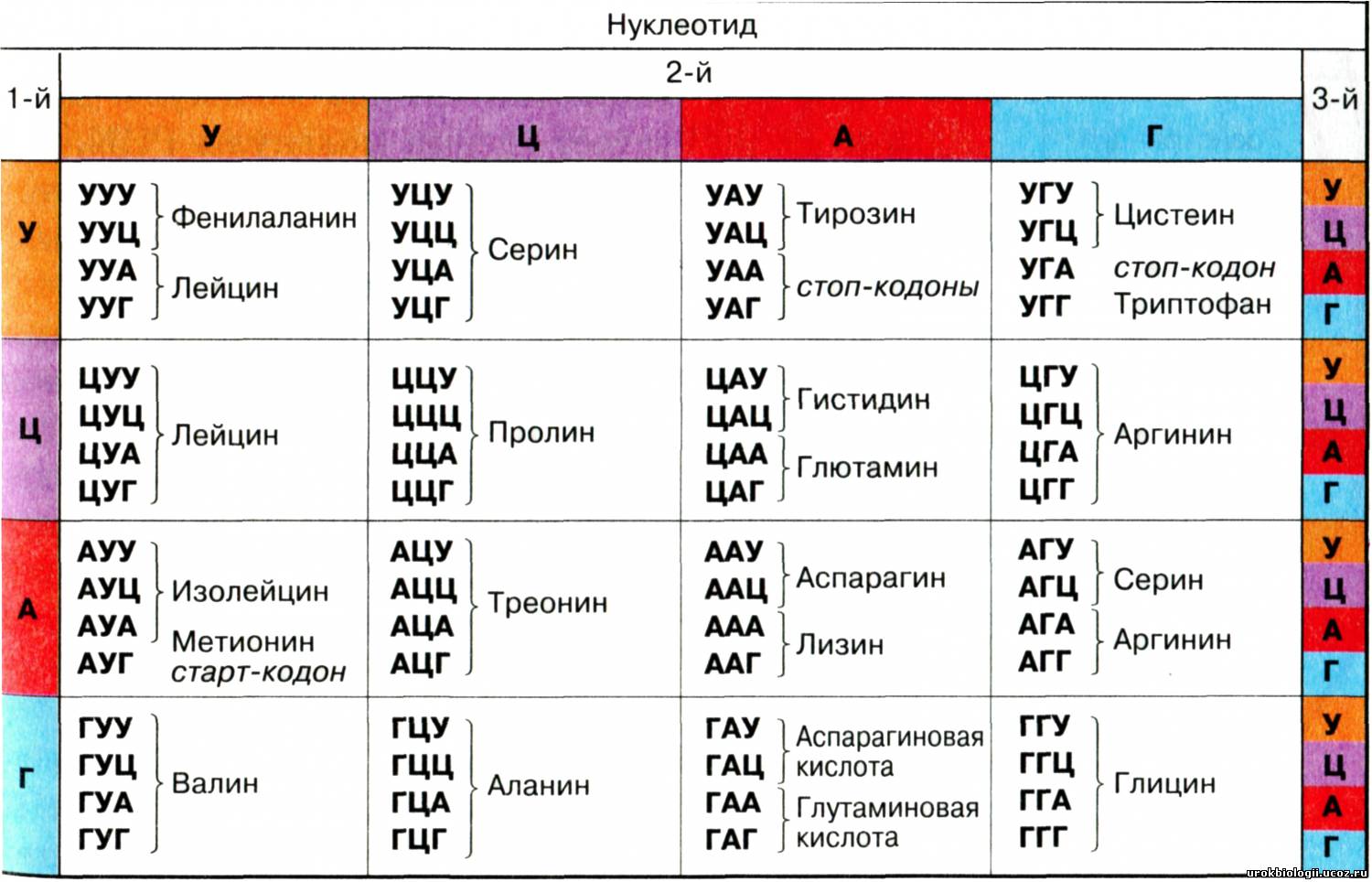
Пожалуй, самым важным открытием генетики является тот факт, что земная жизнь во всех её многочисленных проявлениях произошла от одного и того же предка. Его называют LUCA, или последний универсальный общий предок. И мы можем приблизительно реконструировать его, сравнивая геномы современных организмов и обнаруживая, что у них общего. Главный аргумент в пользу существования LUCA – одинаковая для всех организмов система экспрессии генов (передачи наследственной информации от гена с образованием РНК или белков). Все известные клеточные формы жизни используют один и тот же генетический код из 20 универсальных аминокислот и стоп-сигналов, закодированных в 64 кодонах (единицах генетического кода). Сравнительная геномика показала, что существует 60 общих для всей жизни белков и 355 прокариотических генов, которые восходят к LUCA. По ним можно воссоздать нашего общего предка: LUCA был анаэробным CO2-фиксирующим водородзависимым хемоавтотрофом и экстремофилом, т.е. жил в бескислородной среде, синтезировал органические вещества за счёт энергии, получаемой при окислении неорганических соединений, имел много биохимических путей и мог выдерживать высокие температуры (до 90 градусов).
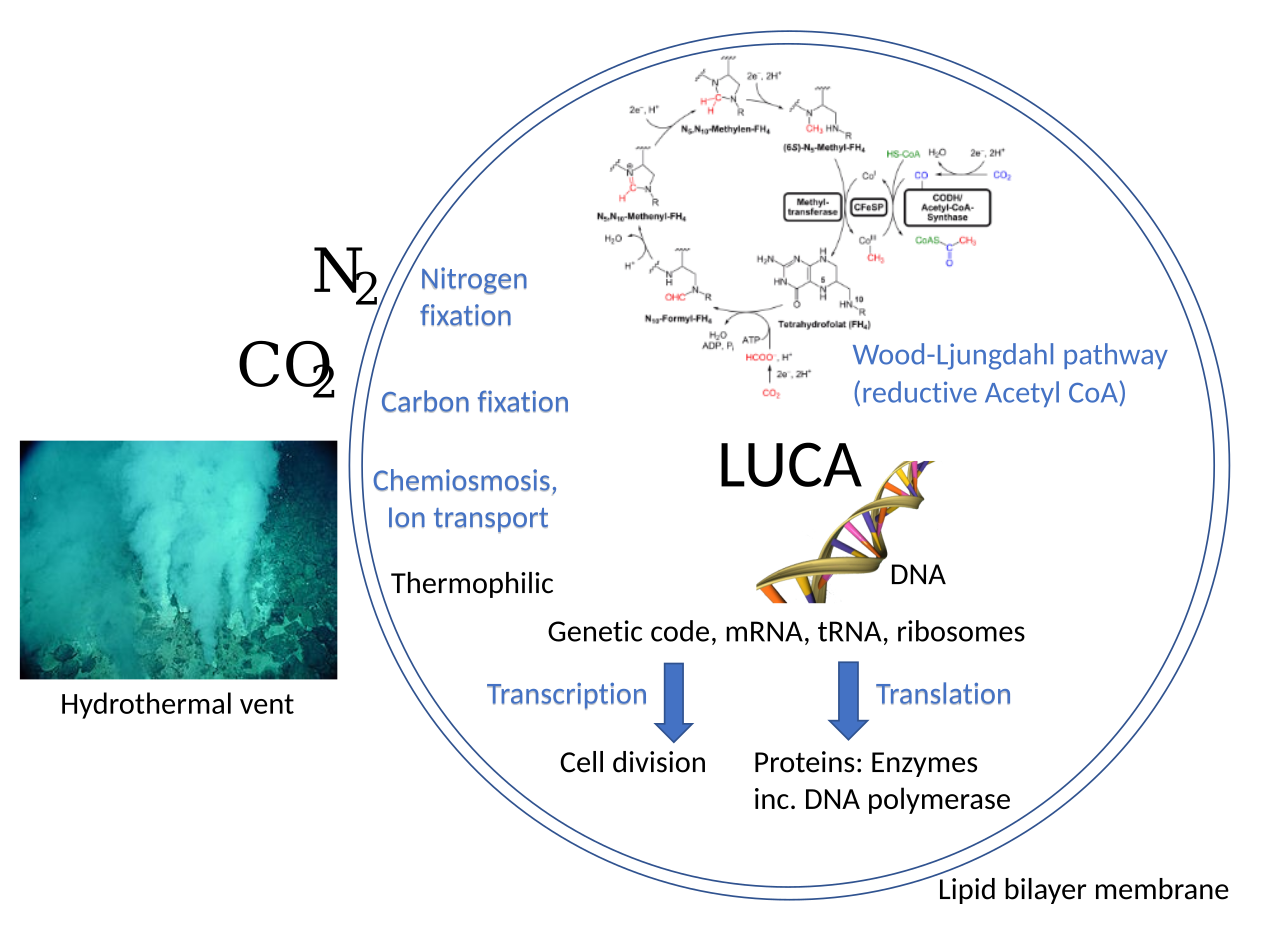
Также известно, что LUCA появился не менее 4 млрд лет назад и представлял собой примитивную прокариотическую клетку с молекулой ДНК длиной около 2 млн пар нуклеотидов, в которой была записана генетическая информация, сохранённая на протяжении миллиардов поколений и благополучно дожившая до наших дней в геномах всех живых существ. Однако генетический код у LUCA отличался от современного (вместо тимина был урацил), механизма репликации ДНК ещё не было (бактерии и археи используют разные ДНК-полимеразы), зато были механизмы транскрипции и трансляции, включая матричную РНК, транспортную РНК и рибосому, которая синтезировала не менее 1300 белков. Среди этих белков были ферменты для осуществления анаэробного дыхания по метаболическому пути Вуда-Льюнгдейла и ДНК-полимеразу для репликации генетического материала. Липидная мембрана сильно отличалась от современных, однако она пропускала ионы металлов и допускала изменение электрохимического потенциала, обеспечивая хемиосмос (превращение энергии цепи переноса электронов в энергию АТФ).
LUCA не был первым одноклеточным организмом на планете и минимальной самовоспроизводящейся единицей, дарвиновская эволюция началась раньше. Скорее всего, вместе с ним жили многие популяции организмов, но только его потомки выжили и сформировали известное палеонтологам древо жизни. В принципе могло бы быть и так, что родословная животных восходила бы к одному предку, растений – к другому, бактерий и архей – к третьему, и т.д. Есть свидетельства, что на ранних стадиях эволюции ключевую роль играл не естественный отбор, а горизонтальный перенос генов, т.е. обмен генетическим материалом между одноклеточными организмами. Но даже этот процесс, не говоря уже о половом размножении, возможен лишь при условии, что геномы участвующих в нём организмов совместимы между собой. Одинаковая структура генетического кода у всего живого однозначно доказывает, что жизнь зародилась лишь однажды. А если это и происходило повторно, то к тому времени наша планета была уже занята, и альтернативные формы жизни не имели никаких шансов выжить в конкуренции с нашими прямыми предками. Последние попросту съели бы любые сложные молекулы до того, как они смогли бы эволюционировать в альтернативную жизнь.
Вероятность жизни. Проблема курицы и яйца
Креационисты любят преувеличивать сложность живой клетки, доказывая, что её сложность неупрощаемая, и она никак не могла быть собрана из более простых компонентов, ведь без каждой из строго подогнанных деталей клетка жить неспособна. Адепты разумного замысла до сих пор цитируют астрофизика Фреда Хойла, однажды сравнившего вероятность самозарождения биологической клетки с вероятностью сборки «Боинга-747» пронёсшимся над свалкой торнадо. Действительно, даже такой примитивный организм, как LUCA, слишком сложный, чтобы случайно собраться из компонентов за разумное время. Мы знаем, что минимальный саморазмножающийся организм Mycoplasma genitalium имеет около 500 генов, каждый длиной примерно 1000 пар оснований. Созданная на его основе синтетическая минимальная клетка JCVI-syn3.0 содержит всего 473 гена, причём функции 149 из них до сих пор остаются неизвестными. Как же такая сложная система могла возникнуть без участия разума?
Задача самосборки клетки из более простых компонентов упирается в проблему курицы и яйца. Что появилось первым: ДНК или белки? ДНК хранит наследственную информацию, белки выполняют всю работу в клетке. Сама по себе ДНК довольно инертна, она не способна ни катализировать химические реакции, ни удваиваться. А белки не являются репликаторами и не могут воспроизводить сами себя. С одной стороны, белки строятся рибосомой по шаблонам, скопированным с ДНК, с другой – для репликации ДНК и выполнения её кода нужны белки – ДНК- и РНК-полимеразы, которые, в свою очередь, образуются путём трансляции гена из ДНК. Как собрать механизм для репликации ДНК, не имея готовой молекулярной программы, то есть инструкции по сборке? И как синтезировать молекулярную программу из миллионов нуклеотидов, не имея готового исполнительного механизма, то есть инфраструктуры, которая должна выполнять синтез? Образуется замкнутый круг, из которого не выйти одной возможностью абиогенного синтеза обоих классов молекул – необходимо ещё и спонтанное возникновение сложной системы их взаимосвязи.
Если простейший репликатор ещё мог появиться за ограниченное время в результате случайных химических реакций, как мы покажем далее, то вероятность случайного возникновения типичного белка из 150-ти аминокислот составляет порядка 1:10195. На это не хватит всех 4.6 млрд. лет истории Земли, за которые можно будет совершить только 1058 попыток. Мы же знаем, что жизнь существовала на планете Земля уже через 500 млн лет после её образования – почти сразу же, как только затвердела земная кора. Даже если взять относительно короткий белок из 87-ми аминокислот 20-ти типов, у нас получается 2087 = 10113 различных вариантов такой аминокислотной цепочки. Если бы даже получили молекулу белка, вероятность получения только ферментов живой клетки за миллиард лет – 10-40000. Отсюда можно было сделать вывод, что за разумные сроки абиогенез невозможен: либо жизнь прилетела на Землю из космоса (гипотеза панспермии), либо была создана искусственно, либо и то, и другое.
Ошибка таких рассуждений заключается в том, что подсчитывается вероятность сборки конкретной последовательности аминокислот методом случайного перебора. Но химическая эволюция – это поэтапный процесс вариации, отбора и накопления удачных вариантов. Некоторые последовательности образуются легче, потому что нуклеотиды и аминокислоты имеют склонность к определённым связям. Существует не одна, а множество функциональных последовательностей, обладающих свойствами фермента или репликатора. Как только появляется молекула с минимальной способностью к самокопированию или катализу, она начинает воспроизводиться чаще, чем другие, запуская процесс молекулярного дарвинизма. Кроме того, событие, которое кажется совершенно невероятным в повседневной жизни, становится вероятным в масштабах наблюдаемой вселенной. Событие, шансы которого составляют 1 к ста миллиардам, вполне вероятно произойдёт где-то во Вселенной, в которой миллиарды галактик с миллиардами звёзд в каждой. Учитывая, что в наблюдаемой вселенной порядка 1021 пригодных для жизни планет, существование жизни хотя бы на одной из них (Земле) возможно даже при условии, что вероятность зарождения жизни составляет 10-20.
Ещё креационисты любят упоминать так называемый «парадокс Левинталя», сформулированный биофизиком Сайрусом Левинталем в 1968 г. Учёный рассчитал, что для короткого белка из 100 аминокислот существует порядка 10100 вариантов его третичной структуры, и если на переход из одной структуры в другую отводить всего 10-13 с, то на перебор всех вариантов уйдёт порядка 1080 лет. Получается, что белок не успел бы свернуться за время жизни Вселенной, а на самом деле он находит самую энергетически выгодную структуру за несколько миллисекунд или минут, в зависимости от длины. Но это происходит только в очень специальных условиях в живой клетке, а в других случаях белки обычно принимают неупорядоченные формы. Даже с новейшими нейросетевыми технологиями алгоритм сворачивания белков на основе искусственного интеллекта AlphaFold2 занимает около 556 ГБ.
К счастью, решение парадокса Левинталя нашёл Алексей Финкельштейн из пущинского Института белка. Он выяснил, что белок не перебирает все варианты, а исключает неподходящие в процессе сворачивания, накапливая упорядоченность. Когда часть цепочки сворачивается в альфа-спираль, этот фрагмент больше не разрушается и не участвует в переборе вариантов, и к нему постепенно присоединяются другие части цепи. В таком случае количество вариантов для белка в 100 аминокислот сокращается до 1067, что даёт наблюдаемое в экспериментах время. Аналогично и для зарождения жизни не нужно случайным образом перебирать всевозможные цепочки, пока случайно не выпадет нужная комбинация из 100 аминокислот, расположенных в строго определённом порядке. Хотя и в случае случайного перебора не обязательно угадывать все 100 аминокислот, достаточно подобрать лишь некий расплывчатый мотив. Среди коротких белковых молекул, искусственно синтезированных путём случайного комбинирования аминокислот, удаётся отыскать белки практически с любой каталитической активностью. Конечно, эффективность таких катализаторов ниже, чем у настоящих ферментов, но отбор со временем доведёт функцию до совершенства. То же самое касается и репликаторов. Именно таким перебором учёные ищут и находят новые рибозимы – РНК с катализирующими свойствами.
Абиогенный синтез органики
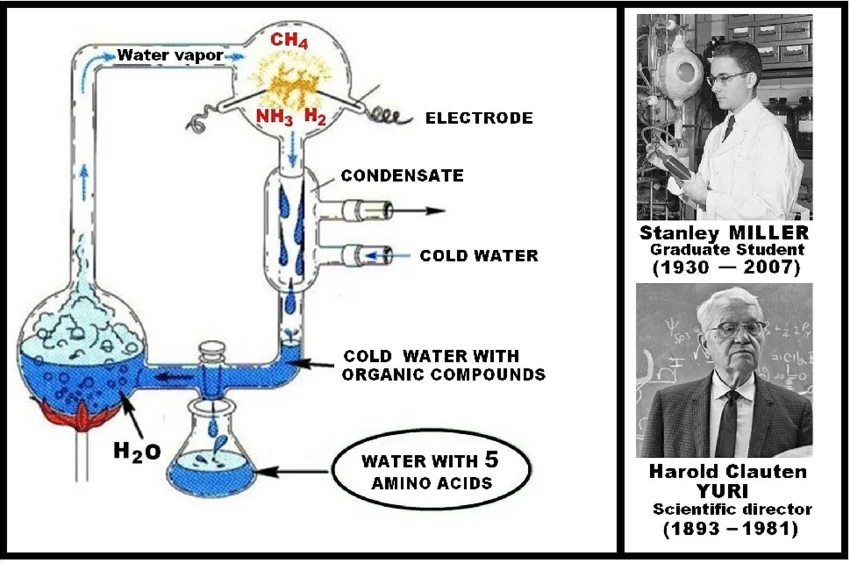
Как не упомянуть в статье о происхождении жизни эксперимент Миллера-Юри? В 1953 г., пока Уотсон и Крик открывали структуру ДНК, Стэнли Миллер и Гарольд Юри провели знаменитый опыт, доказавший возможность абиогенного синтеза органических веществ из неорганических. Они воссоздали в запаянной колбе предполагаемый состав атмосферы ранней Земли (водород, аммиак, метан, водяной пар) и пропустили через эту газовую смесь электрический ток, имитируя удары молний. Через две недели на выходе учёные получили пять аминокислот – органических молекул, из которых строятся белки. Более того, в 2007 г., после смерти Миллера, его студенты заново проанализировали старые колбы, найденные в шкафу Калифорнийского университета в Сан-Диего. С помощью современных методов жидкостной хроматографии и масс-спектрометрии они обнаружили в колбах гораздо больше химических соединений, чем мог выявить сам Миллер, включая 13 из 20 необходимых аминокислот и нуклеотиды для образования ДНК. И всё же ничего более сложного из первичного бульона не появилось. Исследования показали, что атмосфера молодой Земли почти целиком состояла из углекислого газа, азот существовал лишь в форме чистого молекулярного газа (N2), сера – как инертный оксид (SO2), а восстановителей вроде аммиака для фиксации углекислого газа и получения из него хотя бы простейшей органики практически не было.
Давно известно, что аминокислоты синтезируются из формальдегида, синильной кислоты и аммиака в процессе реакции Штрекера, а рибоза – при нагревании водного раствора формальдегида в процессе реакции Бутлерова. Формозная реакция даёт смесь разных сахаров, но исследования показали, что минералы (бор, кальций, глина) и фосфаты увеличивают выход именно рибозы. Проблема нестабильности рибозы решается в условиях сухих циклов (например, на поверхности минералов), где молекулы сохраняются дольше. Азотистые основания нуклеиновых кислот (ДНК и РНК) синтезируются из формальдегида и синильной кислоты, но уже не так легко. Аденин легко присоединяет рибозу, а затем и одну за другой три фосфатные группы, образуя аденозинтрифосфат (АТФ) – универсальную молекулу-носитель энергии. Остальные азотистые основания не удавалось запустить по этому пути несколько десятилетий, пока в 2009 г. группа учёных из университета Манчестера под руководством Джона Сазерленда не продемонстрировала возможность синтеза уридина и цитидина с высокой эффективностью и степенью закрепления результата реакции, а также с возможностью накопления конечных продуктов, в условиях ранней Земли. Они синтезировали активированные пиримидиновые рибонуклеотиды из гликольальдегида, глицеральдегида, цианамида и сероводорода под действием ультрафиолета, без формирования промежуточных звеньев – рибозы и азотистого основания. В 2016 г. было опубликовано исследование, показавшее возможность синтеза всех 4-х рибонуклеотидов из формамида в отсутствие воды под действием ультрафиолета и на поверхности частиц оксида титана, а в 2017 г. была показана возможность самосборки уридина из рибозы, урацила и фосфорной кислоты. Креационистский аргумент о том, что цианид и формальдегид – смертельные яды, неадекватен ситуации, поскольку ни жизни, ни смерти ещё не было. Это обычные реагенты в химии, в малых концентрациях они не разрушают молекулы, а участвуют в реакциях с ними.
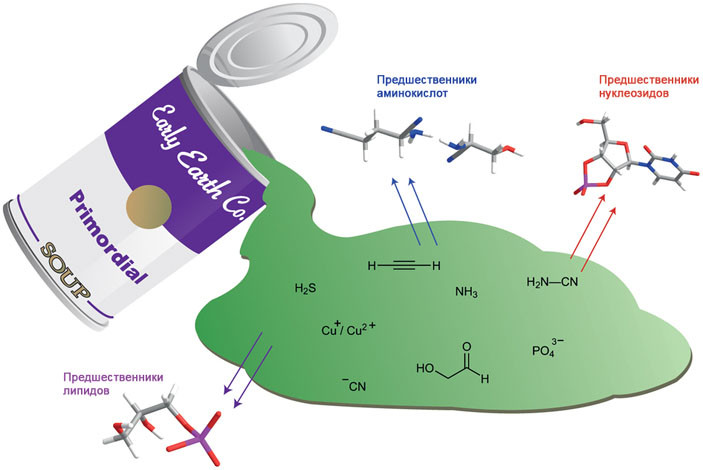
Другой проблемой Миллера-Юри была гомохиральность биомолекул: органические соединения могут существовать в двух зеркально симметричных формах, как правая и левая рука. Химически они равноценны, но белковые ферменты работают не с химией, а с пространственной формой молекул, поэтому правая и левая форма для них различаются, и раз начав с какой-то из них, перейти на другую уже невозможно. Природа почему-то отдаёт предпочтение левым оптическим изомерам аминокислот и правым изомерам сахаров, практически не используя их зеркальные отражения. Все белки построены только из L-аминокислот, а нуклеиновые кислоты – с использованием только D-рибозы и D-дезоксирибозы. Однако в химических реакциях вроде тех, которые моделировали Миллер и Юри, образуется смесь оптических изомеров аминокислот и сахаров. Белок не мог случайно собраться из одних L-аминоксилот, если в смеси присутствует одинаковое количество L и D. Здесь снова подключаются креационисты, заявляя, что вероятность получения аминокислот только левого вращения в белке из 500 аминокислот – порядка 10-160. Очередной шах и мат атеистам?
Нет, играем дальше. Вопреки надеждам креационистов, аминокислоты, найденные в метеоритах из космоса, также являются в основном левосторонними – возможно, это связано с особенностями поляризации ультрафиолетового излучения в молодой солнечной системе. Аминокислоты и сахара не только сами проходят отбор на устойчивость к ультрафиолету, но и образуются под воздействием среды, сформировавшейся под этим излучением. Простой пептидный реликатор может увеличить пропорцию веществ с определённой хиральностью в исходной смеси лево- и правосторонних фрагментов. Согласно другой гипотезе, слабое ядерное взаимодействие, ответственное за бета-распад, производит электроны только с левым спином, и химические вещества, находящиеся под воздействием таких электронов, образуют левосторонние изомеры с гораздо большей вероятностью. В 2011 г. группа Джейсона Хейна из Калифорнии получила хирально чистые рибонуклеотиды стереоспецифическим синтезом, добавляя к системе Сазерленда различные аминокислоты. Было показано, что в присутствии L-аминокислот такая реакция дает преимущественно соединения с D-рибозой. В присутствии гидроксида кальция, цинка и аминокислоты пролина, реакция Бутлерова даёт на выходе только правосторонние сахара. Таким образом, на сегодняшний день все проблемы с абиогенным синтезом необходимых для жизни органических веществ уже решены.
Где зародилась жизнь?
Прежде, чем рассказывать о возникновении первых репликаторов, нужно хорошо представлять себе условия, в которых это происходило. Одним из первых своё мнение о месте абиогенеза высказал Чарльз Дарвин. Он писал о «маленьком тёплом прудике, в котором присутствовали все виды аммиака и фосфорных солей, свет, тепло, электричество и т.д.». Но во времена Дарвина учёные ещё не знали ни истинного возраста Земли, ни механизмов её формирования. Теперь у нас есть косвенные свидетельства о том, что примитивная жизнь существовала на Земле 4.2 млрд лет назад – уже через пару сотен миллионов лет после образования твёрдой коры, в эпоху катархея. Об этом говорят соотношения изотопов углерода во включениях графита в самых древних кристаллах циркона, найденных в Австралии в Джек-Хиллз. В 2017 г. были обнаружены микробиалиты в зеленокаменном поясе Нуввуагиттук на севере Квебека, в полосчатых железистых породах возрастом не менее 3,77 млрд лет, а возможно и до 4,32 млрд лет. Биогенный графит был обнаружен в метаосадочных породах возрастом 3,7 млрд лет на острове Акилия на юго-западе Гренландии и в окаменелостях микробных матов из кремней возрастом 3,49 млрд лет в регионе Пилбара в Западной Австралии.
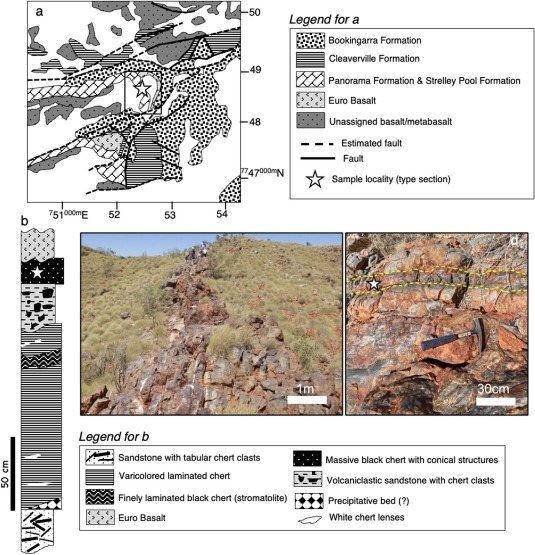
Но в катархее Земля была крайне негостеприимным местом. Она пережила столкновение с меньшей по размерам планетой Тейей, в результате чего от Земли откололась Луна, а также с одной или несколькими кометами, оставившими после себя океаны воды. Поздняя тяжёлая бомбардировка в период от 4,1 до 3,8 млрд лет назад, извержения вулканов, сильнейшие приливы и отливы из-за близкого расположения Луны, токсичная атмосфера из водорода, углекислого газа, азота и метана, беспрепятственный поток солнечной радиации в отсутствие магнитного поля и озонового слоя – все эти факторы сводили вероятность зарождения жизни к нулю. В условиях ранней Земли сложная органическая молекула неизбежно разрушалась бы гидролизом, ультрафиолетом или окислением. Рибоза и пептиды имеют периоды полураспада от нескольких часов до дней. Нуклетиды, такие как аденин, разрушаются за дни-недели. Однако в криогенных или минерал-защищённых условиях, например, внутри астероидов, органические молекулы могут сохраняться миллиарды лет. Так может, у жизни было больше шансов появиться в космосе?
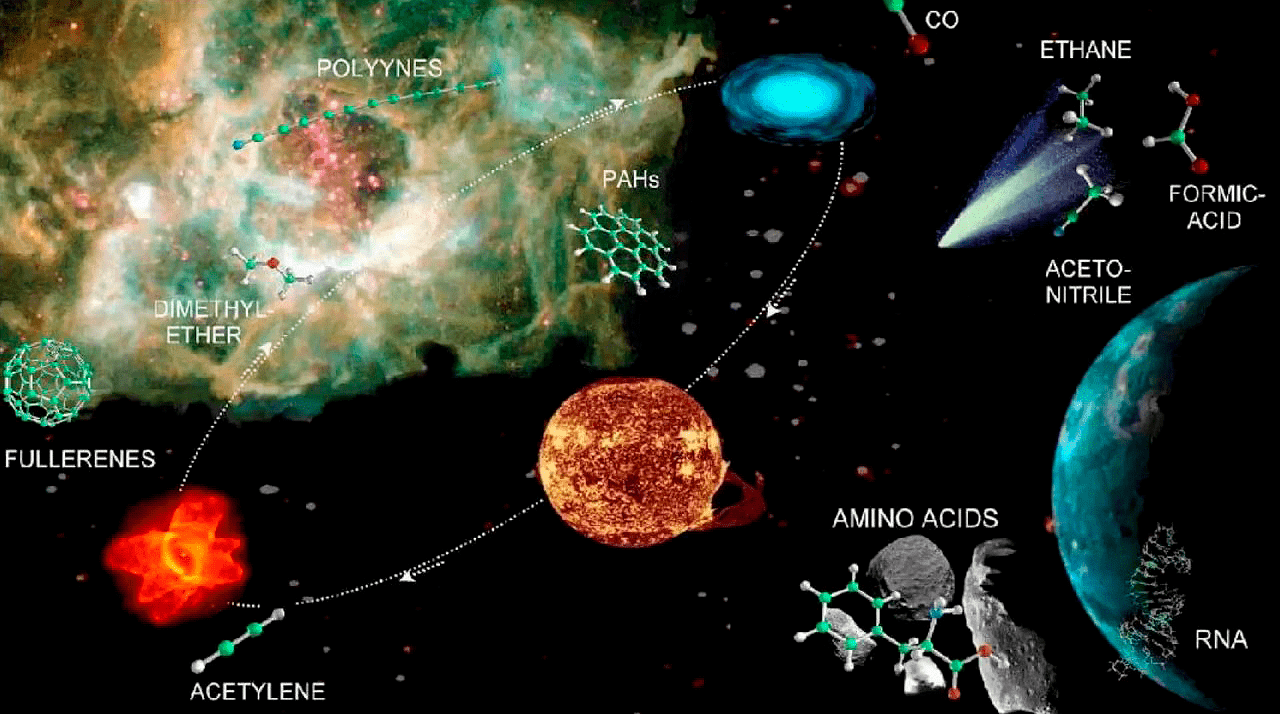
На самом деле молодая Земля – далеко не самое худшее место для зарождения жизни, она имела для этого всё необходимое. Но и космическое происхождение некоторых её компонентов тоже исключать нельзя. Известно, что абиогенный синтез простых органических соединений происходит даже в протопланетном облаке. Простейший углеводород – метан – входит в состав атмосфер многих планет, наряду с углекислым газом, сероводородом, фосфатами и аммиаком. В атмосфере и на поверхности Титана (спутника Сатурна) есть тысячи органических соединений, включая нитрилы и углеводороды. Пуриновые (гуанин и аденин) и пиримидиновые (цитозин, урацил и тимин) нуклеотиды, а также аминокислоты и рибоза, были обнаружены в составе метеоритов. Метеориты типа углистых хондритов содержат более 60 аминокислот, нуклеотиды, полиолы, карбоновые кислоты. В образцах с астероида Бенну, полученных миссией OSIRIS-REx, была обнаружена богатая коллекция органики в солевых растворах в филоcиликaтных минералах, возраст которых оценивается примерно в 4.5 миллиарда лет. Но достаточно ли простых органических молекул, чтобы говорить о наличии жизни, скажем, на какой-нибудь экзопланете?
Как мы убедились в первой части статьи, жизнь требует постоянного потока концентрированной энергии – либо солнечного света, либо тепла и минералов из недр земли. Это исключает из рассмотрения потенциальных мест зарождения жизни глубины океана и места без вулканической активности. Приблизительный химический состав «первичного бульона» можно воссоздать, сравнивая распространённость химических элементов в клетке и в природе. В цитоплазме живых организмов наблюдается более высокие концентрации меди, марганца и цинка, чем во внешней среде. В 2008 г. было показано, что из 49 каталитических доменов, которые содержатся во всех известных организмах, 37 содержат цинк и 19 – марганец. Нуклеотиды, из которых состоят цепочки РНК и ДНК, образуются из азотистых оснований, рибозы и фосфорной кислоты, поэтому в первичном бульоне должно быть много аммиака, метана, фосфора, других органических веществ, водорода и воды. Где можно найти такие условия?
Согласно гипотезе «железо‑серного мира» Гюнтера Ваштерхаузера, жизнь зародилась на океанском дне вблизи гидротермальных источников – т.н. «чёрных курильщиков». Гидротермальные источники и сегодня населяет очень богатая, необычная и практически независимая от внешнего мира жизнь, которая питается «дымом» – перегретой водой, богатой сероводородом и сульфидами. Морская вода около чёрных курильщиков насыщена ионами калия, марганца, магния и цинка, а минералы (апатиты, вулканические породы) обеспечивают доступные формы фосфатов. Анаэробные метаногенные микробы используют в качестве восстановителя сероводород, поступающий из-под земной коры. Все этапы преобразования монооксида углерода в белки могут происходить при высоких температуре и давлении, если катализаторами выступают сульфиды железа и никеля. В таких условиях возможны и более сложные реакции с формальдегидом, гликольальдегидом и цианамидом, ведущие к появлению органических кислот. Осадки сульфида железа могли бы служить и как своеобразные клеточные стенки, и в качестве катализаторов.

Майкл Рассел, Билл Мартин и Ник Лейн считают идеальным местом абиогенеза щелочные гидротермальные источники – «белые курильщики». Это известковые трубы, поднимающиеся со дна океана на высоту до 50 м, полные щелей и отверстий, через которые вырываются тёплые, насыщенные минералами струи воды и метана. Внутри них под воздействием непрерывного потока энергии земных недр образуются завихрения, а что может быть лучше для спонтанной самоорганизации и образования сложных химических соединений? Самые ранние окаменелости микроорганизмов обнаружены как раз в осадках таких гидротермальных источников. Однако в настоящее время версия о зарождении жизни на дне океана считается маловероятной, т.к. в водной среде объединение аминокислот в белки и нуклеотидов в нуклеиновые кислоты не идёт, для этого нужны хотя бы периодически пересыхающие водоемы и воздействие солнечного ультрафиолета, которого на большой глубине нет. Синильная кислота и формальдегид растворимы в воде, поэтому они должны были синтезироваться на поверхности. Также в морской и пресной воде больше натрия, чем калия, а в цитоплазме клеток – наоборот, калия больше чем натрия, много фосфора и цинка.
В 1930-е гг. Александр Опарин предположил, что местом зарождения жизни являются грязевые котлы вблизи вулканов. Они имеют все необходимые микроэлементы, постоянный источник тепла, пористые минеральные осадки в качестве катализаторов и места для концентрации органических соединений, солей и кислот; несколько путей получения органических молекул; фотохимические реакции и расположенные рядом защищённые подогреваемые поры. Как утверждал химик Грэм Кернс-Смит, матрицами для упорядочивания органических молекул могли стать кристаллические структуры, растущие в микропорах глинистых оснований. Циклы увлажнения и высыхания, производимые океаническими приливами, приводят к напряжениям в глине, которые переходят в энергию. Обычная глина может выступать катализатором процесса полимеризации нуклеотидов и аминокислот на защищённых поверхностях пород. Первые самореплицирующиеся молекулы могли сформироваться в маленьких углублениях богатых кремнием поверхностей, а окружающие породы становились для них клеточными стенками. Рассматривая эту гипотезу в своей книге «Слепой часовщик», Ричард Докинз предположил, что микрокристаллы глины и сами могли быть первыми репликаторами. Хотя они не обладали обменом веществ и не реагировали на внешнюю среду, они накапливали информацию и могли размножаться, копируя дефекты своей решётки.

Тем временем Майкл Ярус из Колорадского университета в Боулдере полагает, что химические вещества способны выстроиться в правильном порядке при регулярном замораживании и оттаивании в каком-нибудь слякотном водоёме. В таких условиях лёд обеспечивает концентрацию молекул, стабильность и защиту от распада. В принципе перечисленные гипотезы не противоречат друг другу, если разные стадии абиогенеза проходили в разных условиях. Возможно, дело было так: геотермальные источники (чёрные и белые курильщики) накапливали отложения сульфидов цинка, марганца и других металлов, которые выносились на поверхность вместе с органикой. Здесь, в плотном и горячем воздухе, состоящем в основном из углекислого газа, абиогенный синтез продолжался под действием ультрафиолета, который проникал сквозь атмосферу, ещё лишённую кислорода и озонового слоя. Далее гидротермальные выбросы попадали в грязевые котлы, расположенные в полярных широтах, где происходило как высыхание под действием вулканического тепла, так и замерзание под действием атмосферного холода. Там формировались ледяные глиняные кристаллы, которые послужили матрицами для первых репликаторов. Но на самом деле важнее не где возникла жизнь, а как.
Самоорганизация автокаталитического набора
Один из любимых креационистских аргументов против абиогенеза состоит в том, что информация не может возникнуть сама по себе из шума, а упорядоченная сложность – из энтропии. Здесь происходит подмена научных понятий бытовыми, поскольку в теории информации Шеннона случайный шум как раз содержит максимум информации (энтропии), а упорядоченная последовательность битов предсказуема, поэтому в ней минимум информации. В алгоритмической теории сложности Колмогорова-Хайтина упорядоченность также ассоциируется с простотой алгоритма, а максимальной сложностью обладают случайные строки, которые нельзя сократить. Учитывая, что живая клетка упорядоченнее первичного химического бульона, она имеет более низкую энтропию и несёт меньше информации, соответственно и запрограммировать её должно быть проще, чем смоделировать все химические реакции в предбиотической среде. Но разве код программы не должен быть написан программистом? Не обязательно. Во-первых, потому что мозг программиста является нейросетью, в которой программы создаются по эволюционным алгоритмам или алгоритмам машинного обучения. Во-вторых, потому что программы могут сами появляться в ходе дарвиновской эволюции.
В разработке искусственного интеллекта используется генетическое программирование (ГП) – метод, который автоматически создаёт или модифицирует компьютерные программы для решения задач оптимизации и моделирования, имитируя принципы естественного отбора. Генетические алгоритмы позволяют выращивать популяций программ, которые улучшаются из поколения в поколение путём мутаций, скрещивания и отбора, пока не будет найдено самое адаптивное решение. Задача кодируется таким образом, чтобы её решение можно было представить в виде набора коэффициентов – генов. Первоначально создаётся популяция (набор решений), гены которой определены генератором случайных чисел, затем для каждого варианта решения определяется значение fitness-функции. Fitness-функция – это целевая функция, то есть мера точности решения или мера удовлетворения решению задачи. Увеличением её значения и занимается генетический алгоритм. Отбор идёт по качеству выполняемой функции, а лучшие гены передаются следующему поколению вариантов решений. Используя эволюционные алгоритмы, можно запустить эволюцию программ, играющих в шахматы, шашки, покер, и выполнять практически любые задачи, в которых есть критерий успеха.
Цифровые среды проще реальных физических и химических сред, поэтому смоделировать жизнь на компьютере намного легче, чем в лаборатории. Первым примером небиологического самовоспроизводства стал клеточный автомат фон Неймана, который имел всего 29 состояний в своём пространстве правил. В другом клеточном автомате – игре «Жизнь» Джона Конвея – репликаторы сами появляются из некоторых начальных конфигураций, также возможны конструкции, выполняющие универсальные вычисления, что делает систему полной по Тьюрингу. В 1990 г. Томас Рэй разработал программу Tierra, в которой цифровые организмы жили в общей памяти и конкурировали за вычислительные ресурсы. Эволюция породила паразитов, которые использовали чужой код для размножения, и кооперативные формы поведения, когда программы помогали друг другу. Несколько лет спустя появился настоящий симулятор эволюции – Avida (разработчики – Роберт Пеннок, Ричард Ленски и Чарльз Офрия), в котором цифровые организмы выполняли вычислительные задачи, за что получали «энергию». В результате эволюции возникли программы, способные выполнять сложные логические операции (например, XOR), которые не были заложены напрямую.
В 1992 г. появилась программа Polyworld, написанная Ларри Йегером для развития искусственного интеллекта посредством естественного отбора и эволюционных алгоритмов. В ней популяция из нескольких сотен достаточно сложных трапециевидных агентов ищет пищу, спаривается, производит потомство и охотится друг на друга. После длительной эволюции спонтанно возникает ряд интересных форм поведения, таких как каннибализм, хищник-жертва и мимикрия. Каждая особь принимает решения на основе нейронной сети, использующей хеббовское обучение. Геном определяет структуру нейронных сетей, их размер, скорость, цвет, частоту мутаций и другие факторы. Геном подвергается случайным мутациям с заданной вероятностью, которые также изменяются в организмах-потомках.
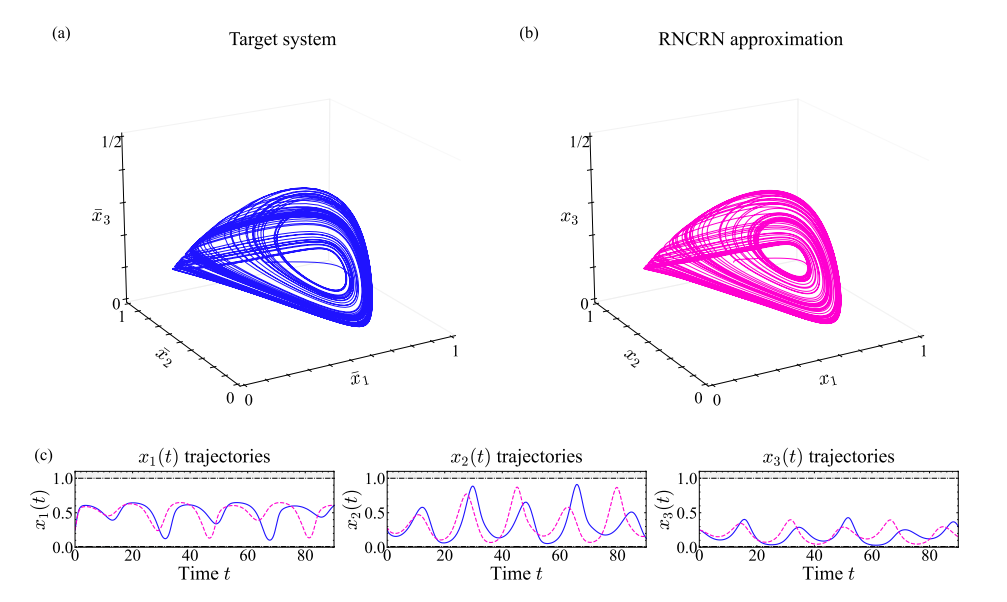
Сеть химических реакций в клетке тоже напоминает нейросеть. Недавние работы по рекуррентным нейронным химическим реакционным сетям (RNCRN) показали, что искусственные рекуррентные нейросети могут быть отображены на химические реакционные сети. RNCRN также могут имитировать произвольные динамические системы, управляемые дифференциальными уравнениями, и, следовательно, аппроксимировать почти любое поведение – от быстрой сигнализации до медленной регуляции генов и контроля клеточного цикла. Этот вывод основан на теореме об универсальной аппроксимации, которая гарантирует, что нейронная сеть достаточного размера способна аппроксимировать любую непрерывную функцию с произвольной точностью. С этой точки зрения, совокупность взаимодействующих молекул превращается в клетку, как только она способна аппроксимировать адаптивные функции, необходимые для выживания.
По сути дарвиновский естественный отбор – это алгоритм поиска геномов наиболее адаптированных к среде организмов. Например, ДНК человека состоит из 3 млрд нуклеотидов, каждый из которых является одной из четырёх букв: А, Ц, Г или Т. Число возможных последовательностей составляет 43000000000, хотя некоторые нуклеотидные последовательности функционально идентичны друг другу, а из абсолютного большинства последовательностей организм бы просто не получился. В любом случае поиск лучшего генома путём случайного перебора невозможно реализовать за разумное время. Однако упрощённая модель эволюции (допускающая смешивание генов путём полового размножения, но не учитывающая мутаций) математически эквивалентна алгоритму мультипликативного обновления весов (MWU), в котором стратегии или гипотезы усиливаются пропорционально их успеху. Аналогичный поисковый алгоритм лежит в основе химической эволюции: при наличии вариации (мутации реакций, концентраций) и отбора (устойчивость, скорость воспроизведения) реакционная сеть будет естественным образом двигаться к более сложным и жизнеспособным конфигурациям. Между химическими реакциями идёт конкуренция за одни и те же субстраты (исходные вещества, необходимые для их проведения). В такой борьбе побеждает та реакция, которая идёт быстрее. Так среди химических процессов начинается естественный отбор: медленные реакции постепенно затухают и прекращаются, вытесняемые более быстрыми.
В книге «Программируя Вселенную» квантовый механик Сет Ллойд пишет, что химические реакции можно рассматривать как разновидность вычисления, если условно принять высокую концентрацию какого-либо вещества в пробирке за 1, а низкую – за 0. Чтобы показать, как вычисляет химия, Ллойд приводит примеры химических аналогов четырёх универсальных логических операций. Когда вещество А усиливает производство вещества В, то есть является катализатором для производства В, это похоже на операцию «копировать»: при А=0 и В=0 на выходе получится 00, а если на входе А=1, В=0, то на выходе реакция даст две единицы (10→11). Обратная ситуация, когда вещество А препятствует производству вещества В – это операция «НЕ»: значение бита В на выходе всегда будет противоположно значению А. Когда концентрация вещества С повышается только при условии участия в реакции высоких концентраций А и В – это операция «И» (11→1, 10→0, 01→0, 00→0). А если высокую концентрацию С можно получить при наличии вещества А или вещества В – это, как нетрудно догадаться, операция «ИЛИ» (11→1, 10→1, 01→1, 00→0). Добавляя в систему всё больше веществ и объединяя перечисленные операции в логические схемы, можно смоделировать любую последовательность химических преобразований.
Таким образом, химические реакционные сети, управляемые кинетикой массового действия, могут симулировать произвольные вычисления и являются Тьюринг-полными. А если сеть способна реализовать универсальные вычисления, то в её пространстве состояний обязательно существуют алгоритмы самовоспроизведения и наследования – генетический код. Минимальная сеть примерно из 10000 компонентов при достаточной связанности и правильном балансе активации и ингибирования может начать вычислять сложные булевы функции. Протоклетка, способная принимать решения, также требует около 10000 взаимодействующих компонентов. Если каждый из них вносит по 10 бит, общий объём информации составляет всего 1 Мб, что соответствуют нижней границы диапазона 106-108 бит информации для минимальной клетки, в зависимости от количества уникальных свёрток, белковых доменов и объёма информации, необходимой для описания каждой из них.
Самоорганизация тесно связана с самореференцией: когда система достигает уровня сложности, на котором она может описывать и воспроизводить саму себя, возникает жизнь. Теория диссипативной адаптации Джереми Ингланда, разобранную в первой части статьи, объясняет, как порядок спонтанно возникает из хаоса в сильно неравновесной системе. Если новая конфигурация имеет низкую энтропию, но позволяет более эффективно рассеивать поступающую извне энергию, она становится термодинамически выгодной и высоко вероятной. Система обучается максимально эффективно использовать внешнюю энергию и рассеивать её в виде тепла, а вместе с тем и записывать информацию о своем окружении и внутреннем состоянии, обрабатывать эту информацию и осуществлять действия, которые положительно влияют на вероятность её выживания и самовоспроизведения. Так по мере роста химического разнообразия происходит резкий фазовый переход – внезапное появление самоподдерживающейся автокаталитической активности.
В 1986 г. Стюарт Кауффман предложил модель автокаталитических наборов реакций – каскадных процессов, в которых каждая реакция создаёт катализаторы для других реакций между веществами данного набора. Когда химические соединения вступают в реакции, некоторые из продуктов этих начальных реакций становятся катализаторами для дальнейших реакций. Концепция автокаталитических множеств объясняет, как химические сети могут самоподдерживаться и усиливать сами себя. Это похоже на цепную реакцию деления урана, где каждое распадающееся ядро излучает нейтроны, вызывающие деление других ядер. Типичный пример автокаталитической реакции – реакция Бутлерова, в ходе которой из формальдегида образуются сахара, которые сами и являются катализаторами этой реакции. После появления в реакционной смеси первых молекул сахаров процесс превращения формальдегида в сахара начинает самопроизвольно ускоряться и становится лавинообразным. Следующий этап – формирование автокаталитических циклов, в ходе которых происходит не только синтез катализаторов, но и частичное возобновление расходуемых субстратов. Вычислительная универсальность автокаталитических наборов означает, что для них существует программа саморепликации, но это не значит, что такая программа проста или её легко найти.
Согласно Кауффману, жизнь возникла не из одной самореплицирующей молекулы, а из первичного автокаталитического набора. Его гипотеза не требует сложно устроенных самовоспроизводящихся высокоточных репликаторов для того, чтобы репликация и обмен веществ (метаболизм) самоподдерживались в среде. В автокаталитических сетях каждая молекула катализируется другим членом множества, что позволяет системе в целом реплицироваться без необходимости, чтобы отдельная молекула самореплицировалась, или чтобы существовала мембранная протоклетка. Уже получены автокаталитические наборы, в которых два фермента (РНК) катализируют синтез друг друга из всего лишь 4 компонентов (нуклеотидов). Первыми саморепликаторами могли быть группы катализаторов: либо белковые ферменты, либо РНК-рибозимы. Такие каталитические циклы могут ограничиваться маленьким прудом или лагуной, либо представлять каталитический комплекс, впитанный либо глиной, либо липидными веществами на глине. Если такие сети ещё и Тьюринг-полны, то они способны не только поддерживать метаболизм, но и реализовывать наследование и адаптацию.
Продолжением модели Кауффмана на биологическую стадию эволюции является теория гиперциклов Манфреда Эйгена и Питера Шустера, разработанная в 1970-е гг. Гиперциклом называют способ объединения самовоспроизводящихся макромолекул в замкнутый автокаталитический химический цикл, где каждая молекула способствует репликации следующей. Тем самым между репликаторами возникает положительная обратная связь, позволяющая преодолеть порог Эйгена – ограничение длины генома из‑за ошибок копирования. Химические гиперциклы уже обладают некоторыми признаками живого: круговорот веществ и энергии, воспроизведение с наследованием информации, приспособляемость к изменяющимся условиям и дарвиновский естественный отбор, но не на уровне видов, а на уровне молекул. Химическая эволюция шла от полукаталитических гиперциклов либо наборов примитивных биохимических путей, включающих приблизительное самовоспроизведение, через полноценные автокаталитические гиперциклы к протоклеточным гиперциклам, в которых клетки также выступали катализаторами, и в конечном итоге к современной биосфере, имеющей все признаки автокаталитического множества.
Гипотеза мира РНК
В 1967-1968 гг. известные биологи Фрэнсис Крик, Лесли Орджел и Карл Вёзе догадались, что ни ДНК, ни белки не являются прародителями жизни. Они обратили внимание на другую молекулу, родственную ДНК – рибонуклеиновую кислоту (РНК). РНК состоит почти из тех же самых азотистых оснований, что и ДНК: аденина, гуанина и цитозина, только вместо тимина в РНК используется урацил. Также отличаются сахара: в РНК это рибоза, в ДНК – дезоксирибоза. РНК – молекула многофункциональная. Она может хранить генетическую информацию (как это делает ДНК), перемещать её (например, из ядра клетки в цитоплазму), а также выступать в роли фермента, катализируя химические реакции. Для хранения и воспроизводства информации РНК недостаточно надёжна, поскольку, в отличие от ДНК, имеет не двойную спираль, а только одну цепочку нуклеотидов. Катализатор из неё тоже не очень, если сравнивать с ферментами-белками. Но РНК является хорошим посредником между «программным обеспечением» клетки и механизмами его реализации: нужный для синтеза ген ДНК служит матрицей для создания одноцепочечной РНК, точно повторяющей структуру этого гена и способной перенести инструкцию по сборке белка из ядра в цитоплазму клетки, где находится рибосома. Основным продуктом трансляции, осуществляемой по коду РНК, являются ферменты. Они управляют всеми регуляторными функциями и химическими процессами в организме, включая процесс репликации ДНК. Но отвечающие за репликацию ферменты ДНК-полимеразы немного различаются у архей, бактерий и эукариот, тогда как процессы транскрипции и трансляции одинаковы. Это значит, что ДНК появилась позже рибосом и системы синтеза РНК, когда три домена жизни уже разделились.
О первичности РНК свидетельствуют многочисленные реликты мира РНК, сохранившиеся в клетках:
-
Рибосома, активный центр которой является рибозимом;
-
Транспортные РНК с характерной формой клеверного листа;
-
Основной носитель энергии в клетках – молекула АТФ, а также некоторые витамины и коферменты (например, НАД и ФАД), являются рибонуклеотидами, а не дезоксирибонуклеотидами;
-
Для запуска процесса репликации ДНК необходим РНК-праймер («затравка»), а для постоянного восстановления концевых участков хромосом (теломер) – фермент теломераза, в состав которого входит РНК-матрица;
-
МикроРНК регулируют экспрессию генов, то есть степень их проявления, посредством РНК-интерференции;
-
Многие вирусы хранят свой генетический материал в виде РНК и поставляют в заражённую клетку РНК-полимеразу для его репликации. Существуют упрощённые вирусы без белковой оболочки, паразитирующие на растениях – вироиды, представляющие собой ни что иное, как самовоспроизводящиеся в клеточной среде кольцевые РНК. Они очень короткие, от 246 до 467 нуклеотидов, тогда как самые маленькие известные вирусы имеют длину генома около 2000 нуклеотидов.
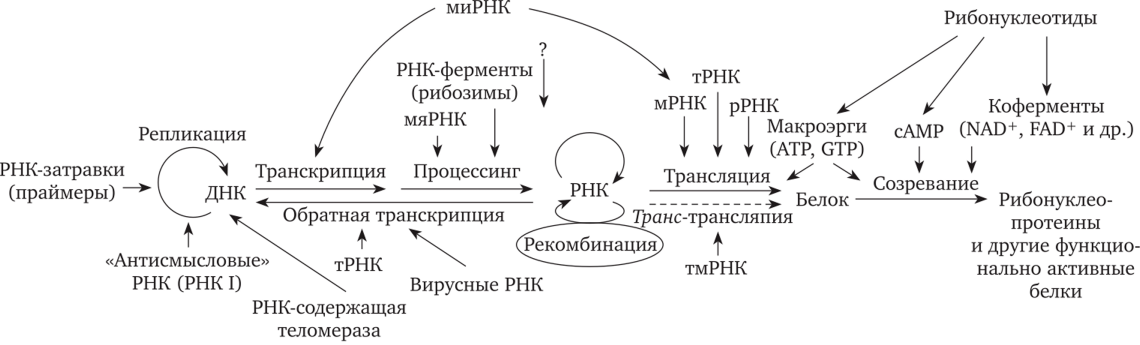
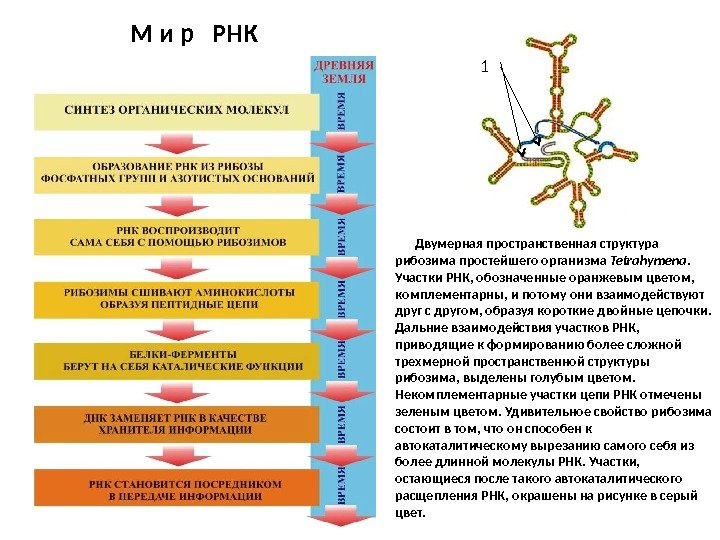
Гипотеза, сформулированная в 1962 г. Александром Ричем и названная «миром РНК» в 1986 г. Уолтером Гильбертом в статье «Происхождение жизни. РНК-мир», говорит о том, что на самой ранней стадии развития жизни в первичном химическом бульоне плавали самовоспроизводящиеся молекулы РНК. Способность РНК как направлять химические реакции, так и служить их катализатором, позволила ей стать первым репликатором. Для этого ей нужно было научиться синтезировать цепочки нуклеотидов без помощи специальных ферментов, отвечающих за репликацию ДНК в наши дни. В 1981 г. Томас Чех открыл РНК эукариота Tetrahymena, осуществляющую сплайсинг самой себя, а в 1984 г. Сидни Альтман доказал, что РНК работает как катализатор – рибозим, способный разрывать или соединять фосфоэфирные связи. Но просто наличия у РНК каталитических свойств ещё недостаточно, чтобы говорить о разгадке происхождения жизни. Для этого нужно как минимум воспроизвести в лаборатории следующие этапы абиогенеза:
-
Абиогенный синтез нуклеотидов из «первичного бульона» простых органических соединений – углеводов и азотистых оснований.
-
Олигомеризация: синтез случайных коротких олигонуклеотидов на минеральных матрицах, с возможным участием аминокислот в качестве катализаторов, в циклах намокания-высыхания в геотермальных системах.
-
Неферментативная репликация – процесс соединения нуклеотидов в короткие молекулы РНК с помощью других РНК и аминокислот, возможно, путём матричного лигирования в слабощелочных условиях. Появляются нуклеопротеиды наподобие современной тРНК или пептидные нуклеиновые кислоты.
-
Возникновение рибозимов, в том числе РНК-полимераз – молекул РНК, катализирующих репликацию других молекул РНК и самих себя. Первые рибозимы-полимеразы могли собраться из нуклеотидов случайно, без помощи наследственности и отбора, а потом они уже эволюционировали по Дарвину, проходя отбор на скорость и точность репликации. У современных организмов таких рибозимов нет, их вытеснили более эффективные белковые полимеразы.
-
Эволюция сложных РНК-организмов и программируемого синтеза белков.
Каковы же экспериментальные подтверждения гипотезы мира РНК?
Первой попыткой запустить дарвиновскую эволюцию РНК был «монстр Шпигельмана» – мутирующая нить вирусной РНК, которую молекулярный биолог Сол Шпигельман реплицировал в подогретом супе из нуклеотидов и полимеризующего фермента репликазы. Однако вскоре он понял, что его молекулы со временем уменьшаются в размерах: копии, которые избавлялись от ненужных генов, реплицировались быстрее, что повышало их шансы на сбор образцов и перенос в новые пробирки для дальнейшего размножения. В 1970 г. Лесли Орджел с коллегами из Калифорнии продемонстрировали химическую эволюцию, добавляя в пробирку с бактериофагом Qβ бромид этидия, ингибирующий синтез РНК. Сначала темп синтеза был замедлен, но примерно после девяти поколений эволюции в процессе естественного отбора вывелась новая порода РНК, стойкая к яду. Последовательным удвоением доз яда была выведена порода РНК, стойкая к очень высоким его концентрациям. Всего сменилось 100 пробирочных поколений (и намного больше поколений РНК, так как поколения сменялись и внутри каждой пробирки). Хотя в этом эксперименте РНК-репликаза добавлялась в раствор самими экспериментаторами, Орджел обнаружил, что РНК способны и к спонтанному самокопированию, без добавления фермента, правда, намного медленнее.
В 1975 г. Манфред Сампер и Рудигер Льюс из лаборатории Эйгена продемонстрировали возникновение РНК из смеси, содержащей только нуклеотиды и Qβ-репликазу. В 1993 г. Дэвид Бэртел и Джек Шостак взяли большой объём произвольной РНК: триллионы молекул, в которых не прослеживалось никаких характерных нуклеотидных последовательностей. Затем выбрали молекулы, которые обладали повышенным каталитическим действием, и сделали множество их копий. Эту процедуру повторили несколько раз: поиск РНК, которая казалась катализатором определённых реакций, и получение её копий. На этапе копирования происходили случайные мутации, и в результате некоторых из них новая РНК становилась более сильным катализатором, чем прежняя. Через десять итераций оказалось, что последний набор молекул катализирует реакции примерно в три миллиона раз лучше, чем исходный.
В 2009 г. Трейси Линкольн и Джеральд Джойс из Скриппсовского исследовательского института в Сан-Диего создали систему из двух РНК-ферментов (рибозимов), которые показали самоподдерживающуюся перекрёстную репликацию. Эти молекулы копировали друг друга примерно за час без помощи белковых ферментов. В результате такой взаимной репликации популяция рибозимов могла размножаться экспоненциально неограниченное время, при условии снабжения растущей популяции материалами для синтеза новых молекул РНК. Правда, в качестве субстрата использовались олигонуклеотиды – довольно длинные фрагменты РНК, состоящие из многих рибонуклеотидов. Но если эволюция РНК начиналась с неферментативного матричного лигирования олигонуклеотидов, то логично, что первые рибозимы-полимеразы тоже продолжали работать с олигонуклеотидами. За 30 часов популяция может в благоприятных условиях вырасти в 100 млн раз. Более того, заставив несколько разных пар размножающихся рибозимов конкурировать друг с другом за субстрат, исследователи вынудили их начать дарвиновскую эволюцию. В результате спонтанных мутаций и естественного отбора появились рекомбинантные рибозимы с повышенной скоростью размножения.
Эволюция рибозимов в автоматизированном устройстве под управлением компьютера наблюдалась в экспериментах Брайана Пегеля и Джеральда Джойса из Исследовательского института имени Скриппса в Калифорнии в 2008 г. Фактором отбора была ограниченность субстрата из олигонуклеотидов и нуклеотидов для синтеза РНК и ДНК. При построении копий иногда случались мутации, влияющие на их каталитическую активность. Самые быстро копирующиеся молекулы начинали доминировать в среде. Затем 90% смеси удалялось, а вместо этого добавлялась свежая смесь с субстратом и ферментами, и цикл повторялся снова. За 3 суток каталитическая активность молекул за счёт всего 11 мутаций увеличилась в 90 раз.
В 2022 г. было обнаружено, что длинные (100-300 звеньев) цепочки РНК образуются при перколяции смеси трифосфатов рибонуклеозидов сквозь вулканическое стекло. В 2024 г. исследователи из Института Солка показали, что РНК-фермент может точно копировать другие функциональные РНК и при этом допускать вариации. В 2025 г. химики из UCL и MRC Laboratory of Molecular Biology показали, что РНК может воспроизводить себя в условиях, моделирующих раннюю Землю. Они нашли способ обойти проблему «залипания» РНК в двойную спираль, которая мешает копированию. А совсем недавно, в феврале 2026 г., учёные из Лаборатории молекулярной биологии MRC в Кембридже под руководством Филиппа Холлигера и Эдоардо Джанни опубликовали в журнале Science результаты своего исследования, в ходе которого они выделили рибозим-полимеразу QT45 (QT – аббревиатура от Quite Tiny – «cовсем крохотный»), состоящий из 45 нуклеотидов.
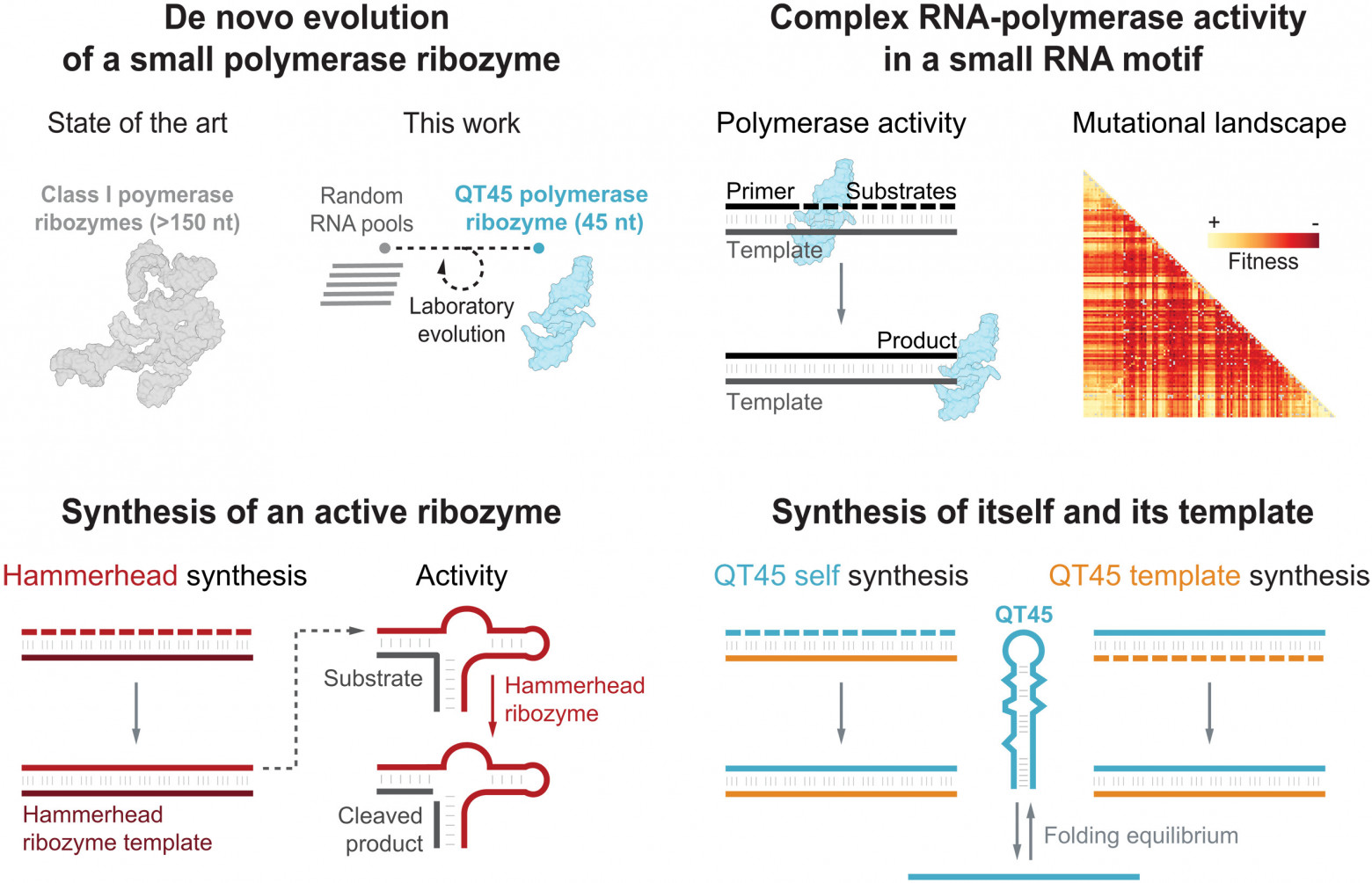
Рибозим-полимераза – это молекула РНК, способная реплицировать другие молекулы РНК. До недавних пор считалось, что получить функциональную самореплицирующуюся РНК без дарвиновского отбора, без использования матричного синтеза и принципа комплементарности, в результате случайной полимеризации нуклеотидов, практически невозможно. Учёным удавалось вывести путём искусственной эволюции или целенаправленно спроектировать только крупные рибозимы-полимеразы длиной более 150 нуклеотидов, ни один из которых не мог реплицировать сам себя. Вероятность случайной самосборки конкретной последовательности из 150 нуклеотидов равна 4150 или порядка 1090, что сопоставимо с числом элементарных частиц в наблюдаемой Вселенной. А молекулы РНК недолговечны, причём длинные, как правило, деградируют быстрее коротких. Для устойчивого самовоспроизводства и эволюции РНК-полимераза должна успеть за свою недолгую жизнь создать хотя бы одну-две полноценные копии самой себя, имеющие не более 2-3 ошибок в каждой.
Теперь, с появлением QT45, минимальная длина цепи сократилась в 3 раза, со 150 до 45 нуклеотидов. Зато пространство всех возможных последовательностей из 45 нуклеотидов – 1027, а это не в три, а в 1063 раз меньше, чем число возможных 150-нуклеотидных последовательностей. С учётом анализа ландшафта приспособленности QT45, его толерантности к мутациям, и того факта, что была изучена только одна из трёх найденных молекул, авторы статьи оценивают вероятность того, что случайная последовательность из 40 и более нуклеотидов окажется РНК-полимеразой, в 1:1016 – это сравнимо с количеством молекул РНК в одной луже первичного бульона.
Среди 10¹³ случайных последовательностей длиной 40-80 нуклеотидов были отобраны те, что присоединяют тринуклеотиды с химическими маркерами в солёной воде со льдом при щелочной реакции. После 11 этапов отбора и мутаций исследователям удалось вывести три непохожих друг на друга коротких рибозима-полимеразы, справляющихся с репликацией разнообразных матриц. Перед отобранными последовательностями ставили всё более сложные задачи, постепенно приближая отбираемые рибозимы к конечной цели: способности реплицировать любые матрицы путем последовательного присоединения комплементарных триплетов. Исследователи использовали в качестве субстратов не отдельные нуклеотиды, а триплеты, которых бывает всего 64.
В экспериментах QT45 помещали в солёную воду, которая при замерзании выталкивала химические соединения в небольшие жидкие участки, где их концентрация повышалась. Молекула использует короткие фрагменты РНК и постепенно достраивает цепь по принципу совпадения оснований. Процесс идет медленно (месяцами), но молекула остаётся стабильной более ста дней. QT45 выполнил синтез рабочей копии 33-нуклеотидного рибозима-эндонуклеазы Hammerhead за 65 дней с выходом 0,39% при точности репликации 92,6%. Но главное, что QT45 за 72 дня успешно синтезировал свою комплементарную реплику (минус-цепь) с выходом 0,24%, используя себя в качестве матрицы, а затем на матрице минус-цепи синтезировал копию себя (плюс-цепь) с выходом 0,17%. Чтобы в процессе цепи не сплелись в двойную спираль, учёные методом проб и ошибок подобрали оптимальную концентрацию триплетов и добавили в смесь один-единственный активированный гексамер (РНК из шести нуклеотидов). Средняя точность репликации минус-цепи составила 94,1% на звено, а доля идеальных плюс-цепей без единой мутации – 43,4%.

Естественно, до создания в лаборатории популяции рибозимов, которая будет без постоянного вмешательства человека жить, размножаться и не вырождаться под грузом мутаций, ещё далеко. Для этого нужны циклические изменения температуры и pH: в тёплой слабокислой среде расплетаются цепи, в слабощелочном льду идёт репликация. Чтобы копируемая последовательность РНК могла эволюционировать под действием отбора, число ошибок должно быть меньше одной на одну копию – это называется предел Эйгена. Если ошибок больше, то естественный отбор не справится даже с сохранением имеющейся генетической информации, не говоря уже о создании новой. Так вот, QT45 всё-таки недостаточно точен, чтобы избежать мутационного коллапса уже в первых нескольких циклах саморепликации. Но исследование повышает правдоподобность идеи об их эволюционном возникновении посредством неферментативной репликации и даже позволяет допустить случайную самосборку готового рибозима-полимеразы.
Согласно другой модели мира РНК, первый репликатор был не одним рибозимом-полимеразой, а содружеством рибозимов-лигаз. Задача лигирования (сшивания коротких РНК в более длинные) даётся рибозимам куда лучше, чем репликация путём последовательного присоединения нуклеотидов. Рибозимы-лигазы получаются легко и в большом разнообразии из случайных коротких последовательностей нуклеотидов. Рибозимы-лигазы, способные к взаимной сборке, склонны самопроизвольно формировать автокаталитические циклы, в которых одни молекулы собирают из компонентов другие. Сообщества рибозимов, основанные на кооперации, побеждают в прямой конкуренции молекулы РНК, собирающие только копии самих себя. Возможно, на каком-то этапе существовали содружества нескольких рибозимов-лигаз и примитивных, неточных рибозимов-полимераз. Полимеразы размножали короткие олигонуклеотиды, а лигазы сшивали из этих олигонуклеотидов более крупные молекулы РНК – копии самих себя и копии полимераз.
Вероятность появления рибозимов-лигаз и полимераз намного выше, если они появились не случайно, а в процессе неферментативной репликации РНК, запустившей дарвиновскую эволюцию. Это могла быть полимеризация случайных коротких РНК на минеральных матрицах или в липидно-нуклеотидном растворе грязевых котлов. Неферментативной репликации свойственна низкая точность и скорость копирования, обычно не превышающая скорость самопроизвольной деградации копируемой матрицы, а также отсутствие праймеров. О том, как решаются эти проблемы, вы можете узнать из лекции Александра Маркова, который предложил в качестве кандидата на роль первого репликатора палиндромную РНК. Она может копироваться с меньшим числом ошибок благодаря своей упрощённой петлевой форме, как у современных транспортных РНК.
Альтернативами миру РНК являются гипотезы о том, что исходными репликаторами были другие нуклеиновые кислоты, которые в ходе дальнейшей эволюции были замещены привычными нам РНК. Кандидатами на роль таких молекул являются искусственно синтезированные, не встречающиеся в живой природе ПНК, ТНК или ГНК. Также существует модель химической эволюции из раствора с «химерами» РНК и ДНК, гипотеза коэволюции РНК и пептидов (мир РНП) и гипотеза вирусного мира.
От репликаторов к протоклеткам
Хорошо, а как тогда из химического бульона с молекулярными репликаторами могла образоваться живая клетка? На этот счёт есть несколько гипотез, самая популярная из которых состоит в том, что первые репликаторы могли обитать в пористых породах на берегах водоёмов. В условиях циклического чередования влажного и сухого периодов (например, во время приливов и отливов) они нуждались в оболочке, защищающей от неустойчивой внешней среды. Сначала они использовали для этого готовые неорганические структуры – минеральные матрицы, а затем путём мутаций обрели способность создавать клеточные стенки. Поскольку такие стенки помогали сохранять нужные для репликации химические вещества в ограниченной области, новая адаптация быстро распространилась по всей популяции самовоспроизводящихся молекул. В экспериментах биолога Дэвида Димера чередование влажности и сухости подтолкнуло липиды к образованию мембран, внутри которых молекулярные фрагменты соединялись в цепочки вроде РНК и ДНК. Липиды при высыхании образуют слои и длинные цилиндры, где последовательности РНК в 50-100 нуклеотидов упорядоченно накапливаются и сохраняют подвижность. В 2008 г. американские учёные создали «протоклетку» с оболочкой из простых липидов и жирных кислот, способную втягивать из окружающей среды нуклеотиды и другие молекулы, необходимые для синтеза ДНК.
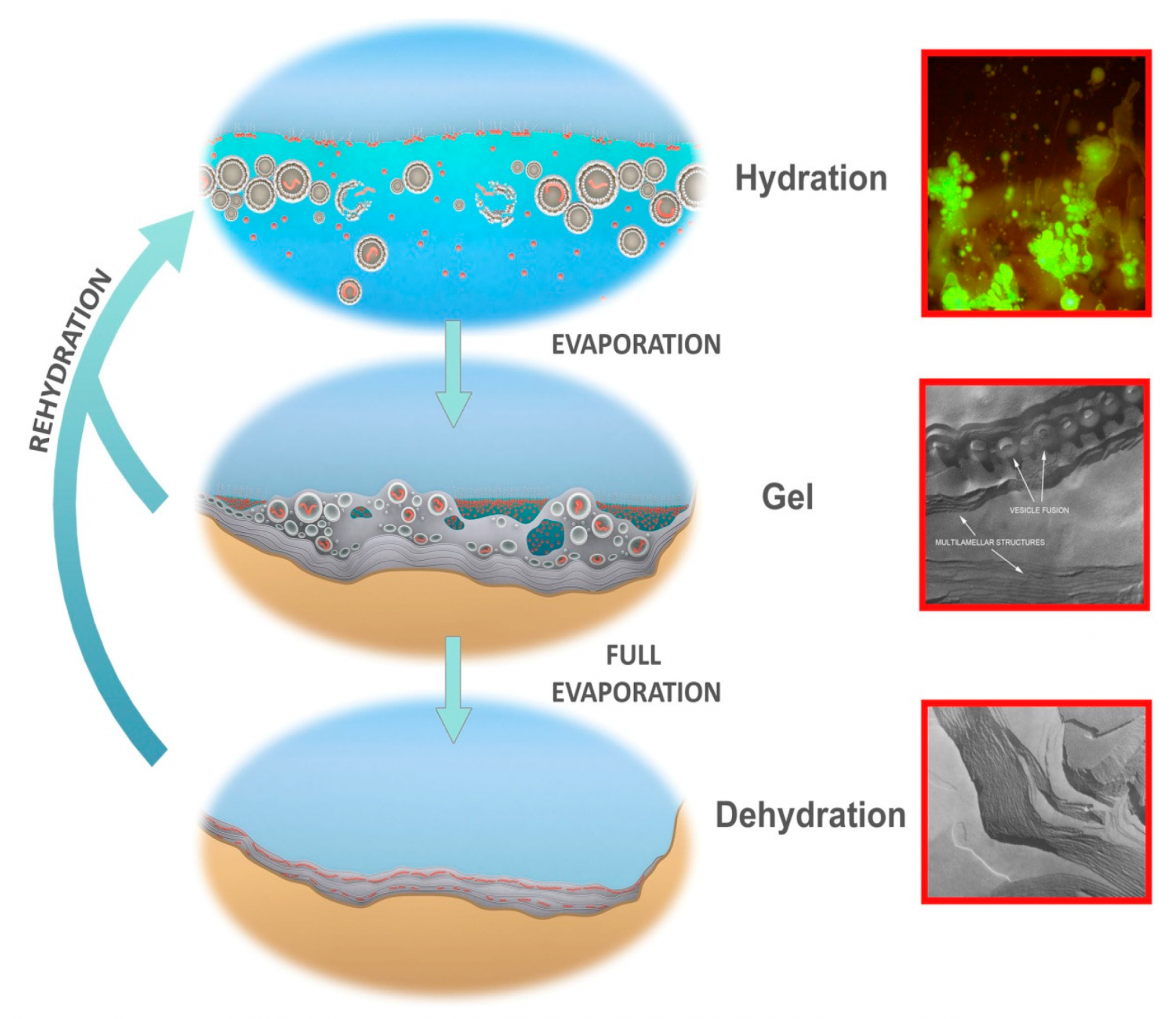
Согласно другой гипотезе, выдвинутой ещё в 1960-е гг. советскими учёными и сегодня развиваемой астробиологом Тони Цзя из Университета Хиросимы, жизнь могла появиться в клейкой слизи, прилипшей к камню – полутвёрдой гелевой матрице, среда внутри которой концентрирует активированные мономеры, способствует их полимеризации, обеспечивает селективное удержание, повышение эффективности реакций и буферизацию окружающей среды. В 1990-е гг. Александр Четверин продемонстрировал, что РНК могут формировать молекулярные колонии на гелях и твёрдых субстратах, где происходил свободный обмен молекулами и химическая эволюция.
У всех живых организмов функцию компартментализации (обособления органелл) обеспечивает клеточная мембрана. Наружная сторона мембраны несёт положительный заряд, а внутренняя – отрицательный. Такой электрический потенциал используется при передаче и хранении энергии, а также транспорта веществ вместе с протонами для компенсации заряда мембраны. Клеточная мембрана включает специальные белки, обеспечивающие выборочное поступление молекул в клетку и из клетки в окружающую среду, а также отвечающие за межклеточную коммуникацию. Сама мембрана состоит из длинных фосфолипидных молекул с полярными гидрофильными головками и неполярными гидрофобными хвостами. Благодаря амфифильности липиды собираются в воде в почти идеальный бислой, где молекулы ориентируются хвостами друг к другу, легко образуя сферические пузырьки – везикулы. Эти пузырьки используются для транспортировки биомолекул через внутриклеточную или межклеточную среду, а на ранних стадиях биологической эволюции они могли служить транспортом для рибозимов. Ограничившись мембраной, жизнь смогла концентрировать внутри молекулы РНК и вести синтез белков, а также перемещаться с потоками жидкости на большие расстояния.

Проблема в том, что мембрана защищает РНК от ультрафиолета и агрессивной химической среды, но при этом изолирует её необходимых элементов – нуклеотидов и ионов. То есть для формирования первых бислоёв с включенной в них РНК уже должны были появиться простые системы закачки или хотя бы связывания нужных элементов. Но каким образом РНК координировала их работу, и как эти белки оказались встроены в мембрану? Полноценная мембрана должна обеспечивать контролируемый обмен веществ. Вероятно, протоклетки имели примитивные оболочки из липидов, которые пропускали протоны и ионы металлов, но задерживали белки и РНК, поэтому выход из геотермальных водоёмов в среду с высоким содержанием натрия потребовал создания клетками способа его откачки – натриевых насосов.

Возможно, оболочки возникли ещё раньше, до появления первых репликаторов. Согласно гипотезе пре-РНК-мира, или липидного мира, или первичной компартмелизации Пьера Луиджи Луизи, в начале появились первичные метаболические протоклетки, а потом уже в них начался синтез реплицирующихся молекул РНК. Эта модель восходит к гипотезе коацерватов («коацерват» в переводе с латыни означает «собранный в кучу»), предложенной Александром Опариным в 1924 г. и независимо от него Джоном Холдейном в 1929 г. Коацерватные капли – это такие пузырьки коллоидной жидкости, окружённые липидными (жировыми) оболочками. Эксперименты Александра Опарина и Сидни Фокса показали, что липосомы и микросферы с мембранными структурами, подобными фосфолипидным бислоям клетки, самопроизвольно образуются в концентрированных растворах белков и нуклеиновых кислот в предполагаемых условиях ранней Земли, а при наличии ферментов коацерват способен к примитивному метаболизму, росту и делению. Из раствора в коацерватные капли поступают химические соединения, которые преобразуются в результате внутренних реакций и выделяются в окружающую среду.
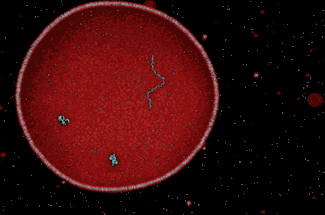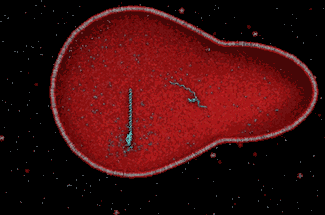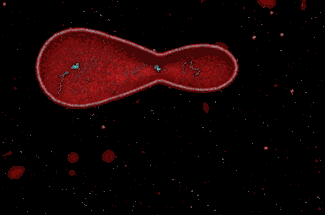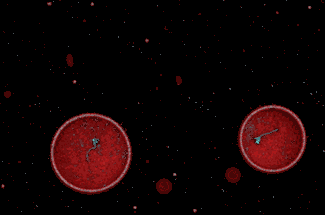
Коацерваты содержат противоположно заряженные пептиды и нуклеиновые кислоты, которые скапливаются в каплях благодаря электрохимическому контакту между молекулами. Но собственная мембрана у них не формируется, поэтому коацерватам требуется дополнительный стабилизатор, иначе они активно сливаются с другими коацерватными каплями и обмениваются молекулами, что препятствует межклеточной конкуренции, отбору и закреплению полезных мутаций РНК. В 2022 г. группа учёных из Иллинойса и Миннесоты под руководством Амана Агравала показала, что коацерватные капли можно стабилизировать и не допускать их слишком быстрого перемешивания, если подмешивать их в деионизированную воду. Агравал более двух лет пытался смоделировать раствор с нужной кислотностью, пока не вступил в коллаборацию с химиками из университета Хьюстона Мэтью Тирреллом и Джеком Шостаком. В 2024 г. в журнале Science Advances они опубликовали статью, в которой показали, что целостность коацерватных капель обеспечивает обычная дождевая вода из Хьюстона.
В конце 2023 г. Цяо Янь из Института химии китайской Академии Наук, Юань Линь из Пекинского университета химических технологий и Стивен Манн из Бристольского университета опубликовали совместную статью, в которой рассказали, как они целенаправленно настраивают протоклетки для имитации различных клеточных функций: химической сигнализации, морфологической дифференциации, экспрессии белков, запасания энергии. Протоклетки собирают из разных сортов коацерватов, заранее рассчитывая форму и последовательность их слоёв. Протоклеточная структура спонтанно сортируется на упорядоченные слои жидкокристаллических коацерватов и неупорядоченные микрокапли. ЖК-коацерваты селективно впускают в себя белки, полисахариды, липиды и АТФ, а в неструктурированных коацерватах концентрируются нуклеиновые кислоты. Так учёным удалось смоделировать две взаимопроникающие среды, одна из которых отвечает за биохимические реакции, а другая – за хранение генетического материала.
В рамках гипотезы РНК-пептидного мира утверждается, что короткие нуклеотидные цепочки и аминокислоты могли образовываться и полимеризоваться без участия ферментов только в очень небольших протоклетках, которые при этом могли бы сливаться друг с другом, не нарушая уже идущих биохимических реакций. Коацерватные капли очень хорошо подходят на роль таких первичных биологических пузырьков, поскольку смешиваются друг с другом и при этом не смешиваются с водой. Белки стали промежуточным звеном построения липидной оболочки, а эволюция плоских структур РНК, превратила их в трёхмерные скопления, покрытые мембраной. В 2011 г. японские учёные поместили элементы ДНК внутрь везикул с катионной оболочкой и добились запуска полимеразной цепной реакции, реплицирующей ДНК. Но в этих опытах использовались белковые ферменты, которых в первичном бульоне могло и не быть. Поэтому более многообещающей кажется гипотеза неферментативной репликации РНК внутри липидных везикул.
Первые попытки неферментативной репликации РНК осуществил в 1980-х гг. Лесли Орджел, добившись копирования матрицы из 14 нуклеотидов гуанина и цитозина. Сегодня его идею развивает химик Джек Шостак из медицинской школы Гарвардского университета, полагая, что репликаторы появились в каплях жира – в воде, заключённой в липидную мембрану. В 2003 г. Шостак добился ускорения образования везикул в 100 раз, используя в качестве катализатора глинистый минерал монтморилонит. В 2012 г. Шостак показал, что смесь нуклеотидов РНК и ДНК может собираться в «мозаичные» молекулы-химеры, по каталитическим свойствам аналогичные рибозимам. Проблема в том, что для реакции репликации требовались ионы магния, которые могли разрушать протоклетку. Но в 2013 г. Джек Шостак и Катаржина Адамала добавили в искусственную протоклетку цитрат (соль лимонной кислоты), в результате чего она смогла самостоятельно воспроизводить молекулу РНК без разрушения мембраны. В 2016 г. команда Шостака смешала в одном растворе шаблон РНК со свободно плавающими фрагментами РНК. Некоторые из этих фрагментов соответствовали частям шаблона, но в растворе не было ферментов, необходимых для репликации. Тем не менее, команде удалось получить достаточно точные копии шаблона.
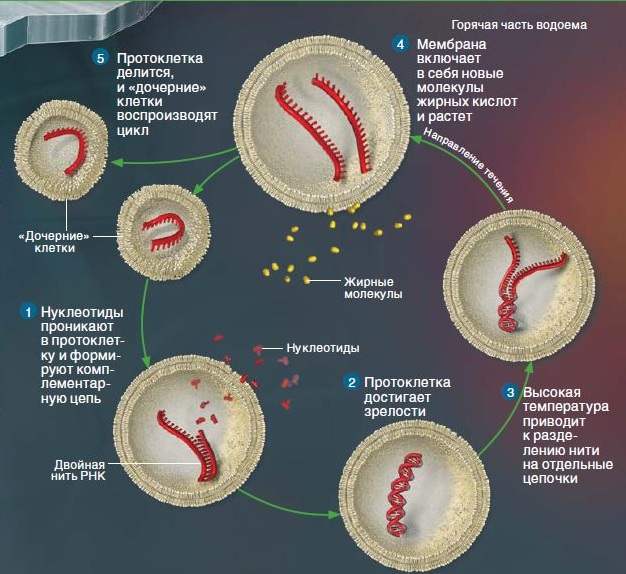
Джек Шостак предлагает модель коэволюции РНК и мембраны, согласно которой первые пробионты могли быть сообществами абиогенно синтезированных липидов и рибозимов. При низкой температуре липидная оболочка пропускает внутрь нуклеотиды, они соединяются в двухцепочечную РНК и не могут выйти наружу, а при высокой температуре РНК расплетается на отдельные цепи, а вместе с ней делиться и протоклетка. В результате между РНК и двухслойными везикулами из жирных кислот сложился симбиоз: мембрана защищала РНК и продлевала ей жизнь, чтобы она успела реплицироваться, а РНК привлекала на мембрану другие биомолекулы, в результате чего мембрана росла и делилась надвое. Далее, согласно гипотезе Ирен Чен и Джека Шостака, элементарные протоклетки освоили примитивные формы размножения, конкуренции и накопления энергии. Конкуренция за молекулы обеспечила селективное преимущество для сшитых жирных кислот и современных фосфолипидов. В зонах тектонических разломов в земной коре циклическое давление периодически формирует везикулы, а также случайные пептидные цепи, которые отбираются по способности интегрироваться в мембрану везикулы. Отбор самих везикул по стабильности мог привести уже к функциональным пептидным структурам.
От мира РНК к миру ДНК и белков
Итак, у нас есть молекула РНК, заключённая в проницаемую липидную оболочку, неточно копирующая другие РНК и саму себя. Но разве это жизнь? Одноразовое копирование последовательности нуклеотидов или коацервата ещё нельзя назвать полноценной репликацией – это просто случайное совпадение. Чтобы информация воспроизводилась, нужен механизм обратной связи – молекулярная память. Как утверждает Филипп Холлигер из Лаборатории молекулярной биологии MRC в Кембридже, «у биологии есть память, а у химии её нет», поэтому первоосновой жизни всё-таки должен быть генетический код. А как же проблема курицы и яйца? Конечно, все давно знают, что яйцо древнее курицы, но речь не об этом. Что возникло раньше: ДНК или копирующий её механизм? И как они могли существовать по отдельности, если это единая система с обратной связью?
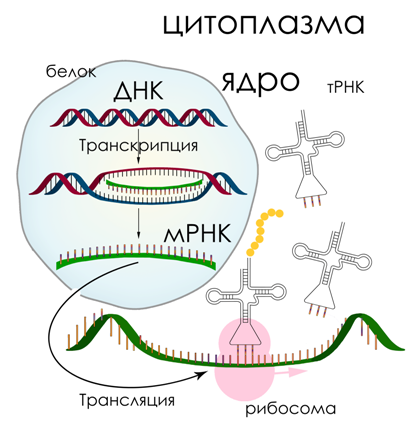
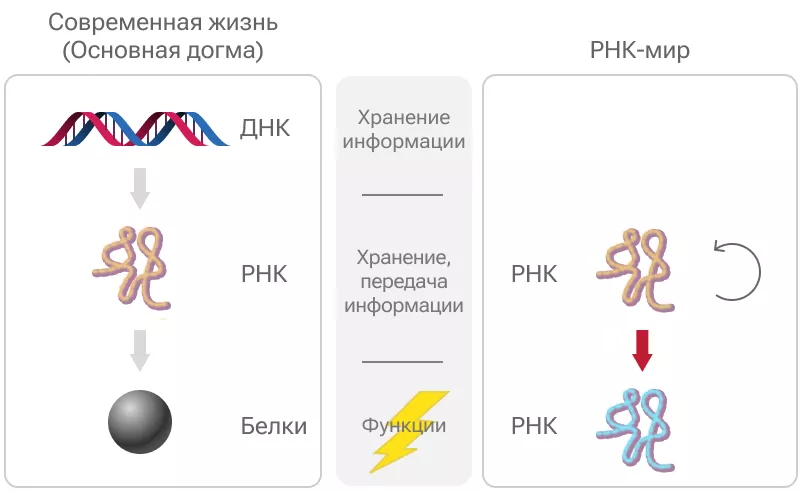
Переход от мира РНК к миру ДНК и белков произошёл благодаря химической эволюции – молекулярному дарвинизму. РНК уже могли существовать полностью автономно, катализируя метаболические реакции (например, синтеза новых рибонуклеотидов) и самовоспроизводясь, сохраняя из поколения в поколение каталитические свойства. При каждом копировании в структуре РНК происходили случайные мутации, и некоторые из них позволяли РНК собирать из окружающих её аминокислот примитивные короткие белки – пептиды. Если эти белки, катализируя химические реакции, повышали эффективность репликации РНК, то мутировавшая РНК получала преимущество перед конкурентами. Она активнее распространялась в окружающей среде и синтезировала в ней всё больше белков, а те, в свою очередь, способствовали дальнейшей её репликации. Так формируется положительная обратная связь, грубо воспроизводящая процессы, происходящие в рибосомах клеток. Затем на протяжении миллионов лет естественный отбор закреплял ошибки и мутации, повышающие адаптацию репликатора к среде.
До сих пор биосинтез белка в природе почти полностью осуществляется с помощью различных РНК: матричные РНК являются матрицей для синтеза белка в рибосомах; транспортные РНК считывают генетический код и доставляют аминокислоты к рибосомам; рибосомная РНК составляет активный центр рибосом, катализирующий образование пептидной связи между аминокислотами. Универсальный конструктор белков – рибосома – состоит из примерно 70 белков и трёх молекул РНК общей длиной до 5000 нуклеотидов. Кроме того, для работы рибосомы нужна система подачи активированных аминокислот, которая включает в себя примерно 40 типов транспортных РНК, 20 типов ферментов (аминоацил-тРНК-синтетаз), и еще десяток вспомогательных белков (факторов инициации, элонгации и терминации). Рибосома считывает нуклеотиды с РНК, подбирает аминокислоты согласно генетическому коду и нанизывает их одну за другой, создавая белок.
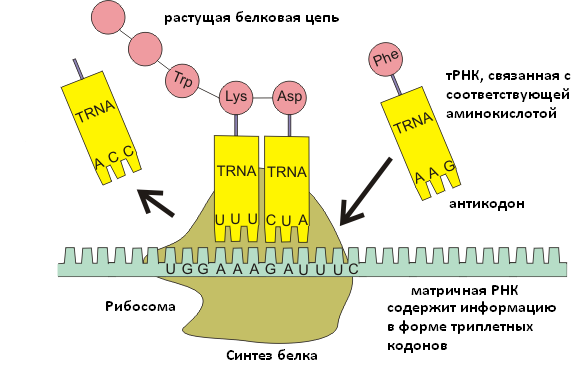
Всё это кажется неупрощаемо сложной системой с явными признаками «разумного замысла». Но в действительности рибосома – весьма архаичная и примитивная машина родом из мира РНК, которая прошла миллиарды лет практически без усовершенствований, поскольку большинство изменений сразу же приводили к ошибкам в синтезе белков и как следствие – к нежизнеспособности организма. Рибосома работает с КПД меньше 10%, расходуя 4 макроэргические связи (молекулы АТФ и ГТФ) на формирование одной пептидной связи, и рассеивая 90% энергии в виде тепла. Кроме того, рибосома ищет нужную тРНК, просто перебирая молекулы, которые случайно сталкиваются с её активным центром: в среднем от 10 до 30 тРНК примеряются к очередному кодону, прежде чем найдётся правильная. Бактериальная рибосома синтезирует белок со скоростью ~15-20 аминокислот в секунду, при этом ошибки встречаются примерно раз на 10³-10⁴ аминокислот. Большинство ошибок приводит к нефункциональным белкам, которые приходится утилизировать.
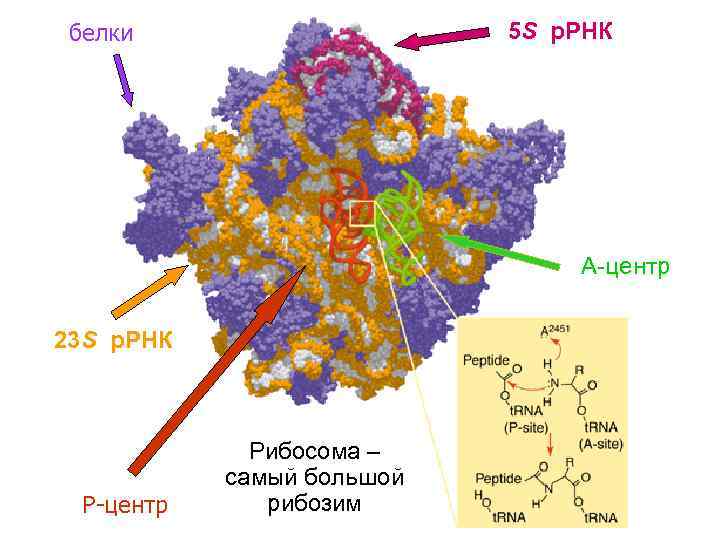
Рибосома делится на большую и малую субъединицы, которые эволюционировали отдельно. В структуре большой субъединицы рибосомы выделяются чётко выраженные слои, различающиеся содержанием ионов магния и белков, а также структурой контактов между участками самой РНК. Это явно указывает на то, что они имеют разный эволюционный возраст, что и было подтверждено расшифровкой трёхмерной структуры рибосомы в 2001 г. Активный центр рибосомы, который катализирует образование пептидных связей, состоит из одной рРНК, а белки не играют существенной структурной роли и имеют периферийное функциональное значение. Рибосомная РНК состоит из относительно самостоятельных фрагментов – доменов, отделяя которые в определённом порядке, можно разобрать рибосому как конструктор. В 2009 г. биохимики из Монреальского университета Константин Боков и Сергей Штейнберг, изучив основную составляющую рибосомы бактерии Escherichia coli, молекулу 23S-рРНК, показали, как из небольших и простых рибозимов мог развиться механизм белкового синтеза. Методом искусственной эволюции были получены функциональные рибозимы, способные катализировать транспептидацию, очень близкие по структуре к предполагаемой проторибосоме.
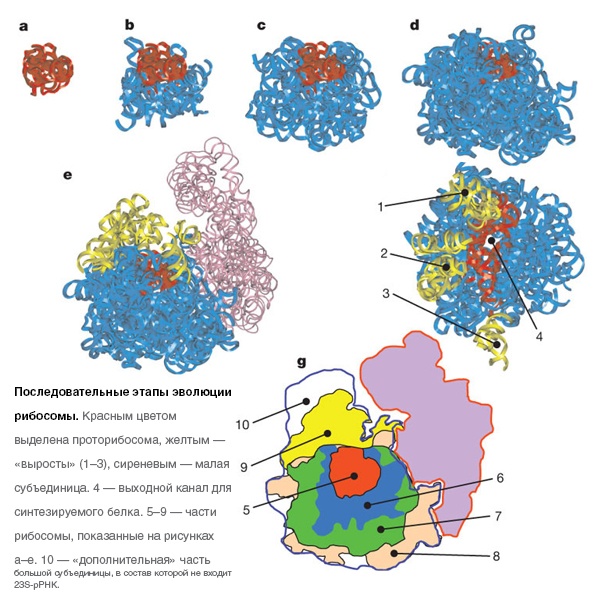
Оказывается, рибосома эволюционировала из более примитивного рибонуклеопротеинового аппарата – пептидилтрансферазного центра (5-го домена рРНК), присоединяющего новые аминокислоты к растущему пептиду. Такой рибозим способен синтезировать белковые цепочки из отдельных аминокислот, пусть и неточно, медленно, особенно в сравнении с современными сложными биохимическими системами, и без соответствия матричной РНК. Но как способность синтезировать случайные пептиды помогла рибозиму выжить и вытеснить конкурентов, включая тех, которые катализировали появление собственных копий? Дело в том, что в мире самовоспроизводящихся РНК нуклеотиды были дефицитным ресурсом, и некоторые рибозимы стали «красть» их, гидролизуя соседей. В результате эволюционное преимущество получили те репликаторы, которые могли связывать аминокислоты в короткие положительно заряженные пептиды, которые помогали работать отрицательно заряженным рибозимам. Известно, что многие белки, образующие альфа-спираль, могут неспецифически связываться с двуспиральной РНК, тем самым защищая её от гидролиза щелочами, ионами металлов и ферментами РНКазами. Последовательность аминокислот практически не важна – пептид случайной последовательности уже обеспечивает заметную защиту. Такие случайные пептиды могли связываться с одноцепочечными полимерами нуклеиновых кислот, повышая их стабильность. Это спровоцировало «гонку вооружений»: «хищные» рибозимы научились расщеплять белки, а «жертвы» стали усложнять состав аминокислот в защитных пептидах. Далее отбор способствовал переходу от простого регулярного чередования нескольких аминокислот к сложным последовательностям пептидов, для чего понадобился матричный синтез. Так появились мРНК, тРНК и генетический код.
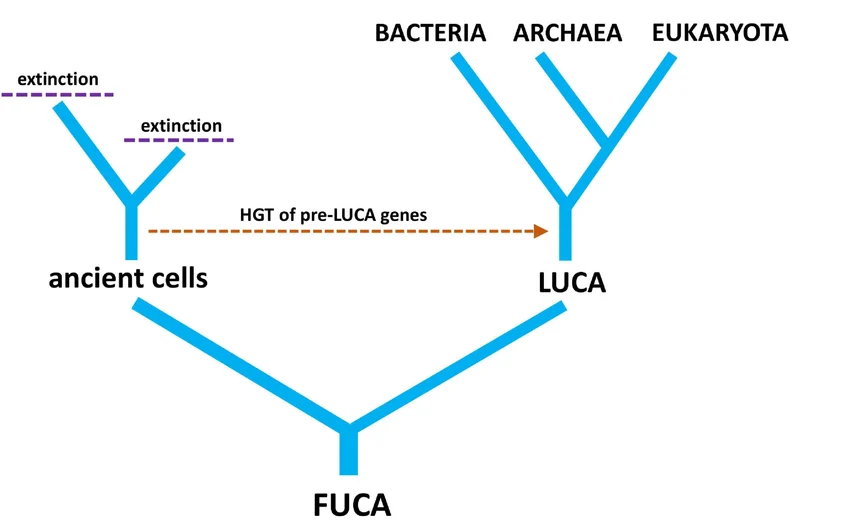
После образования рибосомы на сцену выходит первый универсальный общий предок –FUCA. В отличие от последнего общего предка всех ныне живущих организмов (LUCA), это был ещё неклеточный организм, предшествовавший как бактериям, так и вирусам. Но он был первым носителем полноценного генетического кода, способным осуществлять биологическую трансляцию молекул РНК для образования белков посредством синтеза пептидов. Первые гены, скорее всего, кодировали рибосомные компоненты, примитивные тРНК-аминоацилтрансферазы и другие белки. Возможно, вам всё ещё кажется удивительным, как случайные химические флуктуации могли породить сложный генетический код из 64-х «слов» (комбинаций из 4-х оснований по 3 в каждом кодоне), который стал универсальным для всех живых организмов. Креационисты говорят, что генетический код – сверхсложный абстрактный язык, явно сотворённый разумом, потому что кодоны не имеют химического сродства с аминокислотами: можно представить, что те же кодоны кодируют другие аминокислоты, а аминокислоты кодируются другими кодонами. Но условность и универсальность генетического кода может быть и результатом закрепления отбором наиболее устойчивой и помехоустойчивой системы в ранней биосфере.
В популярном представлении геном является своего рода чертежом и программой клетки, кодирующей все её органеллы и функции. Но в действительности это просто инструкция по сборке белков – в геноме не написано, какой белок что делает. Гены – не более чем строки кода, регуляторные элементы работают как условные операторы, определяя, когда и где включается синтез белков, белки – это функции программы, которые выполняют задачи (катализируют реакции, строят органеллы, передают сигналы), а органеллы – модули или библиотеки в программе, где функции объединяются для выполнения одной сложной задачи. Бактериальная клетка очень далека от совершенства, что бы ни говорили креационисты. У типичной бактерии с ~4-5 тыс. генов происходит около 10⁻⁹ мутаций на ген за поколение, т.е. в каждой популяции из миллионов клеток будут появляться десятки новых мутаций в каждом поколении. Большинство мутаций оказываются губительными, но некоторые позволяют адаптироваться к новым условиям среды, поэтому бактериям с их быстрым циклом самовоспроизводства выгодно часто мутировать. Эукариоты научились защищаться от мутаций с помощью избыточного кода и механизмов коррекции ошибок, но это стало причиной множества других «багов», которые мы уже рассматривали в статье «Правда и мифы об эволюции».
У простейших РНК-репликаторов одномерная последовательность нуклеотидов кодирует трёхмерную форму молекулы. Чтобы стать рибозимом, РНК сворачивается за счёт попарного соответствия оснований (комплементарности) – это и есть элементарная форма считывания «текста» РНК. С появлением в результате отбора белкового синтеза, РНК-полимераза сняла с рибозимов обязанность репликации и позволила увеличить количество генетической информации. Появились матричные РНК белков для копирования РНК, прото-рибосомные РНК для синтеза белков и транспортные РНК для связывания кодонов с той или иной аминокислотой. Показано, что ди- и трипептиды могут быть синтезированы с помощью системы, состоящей только из аминоацилфосфатных адаптеров и РНК-направляющих. В экспериментах были отобраны аминоацилирующие рибозимы, способные заряжать тРНК соответствующими аминокислотами. Код возник при объединении двух автокаталитических сетей – РНК и пептидов. Сначала могли существовать молекулы, которые связывали аминокислоты с короткими РНК. Постепенно такие системы усложнялись, пока не возникла универсальная схема трансляции – сопоставление нуклеотидных триплетов и аминокислот. Соединения РНК с пептидами (рибонуклеопротеины) эволюционировали в белки, лучше выполняющие каталитические, транспортные, структурные и сенсорные функции.
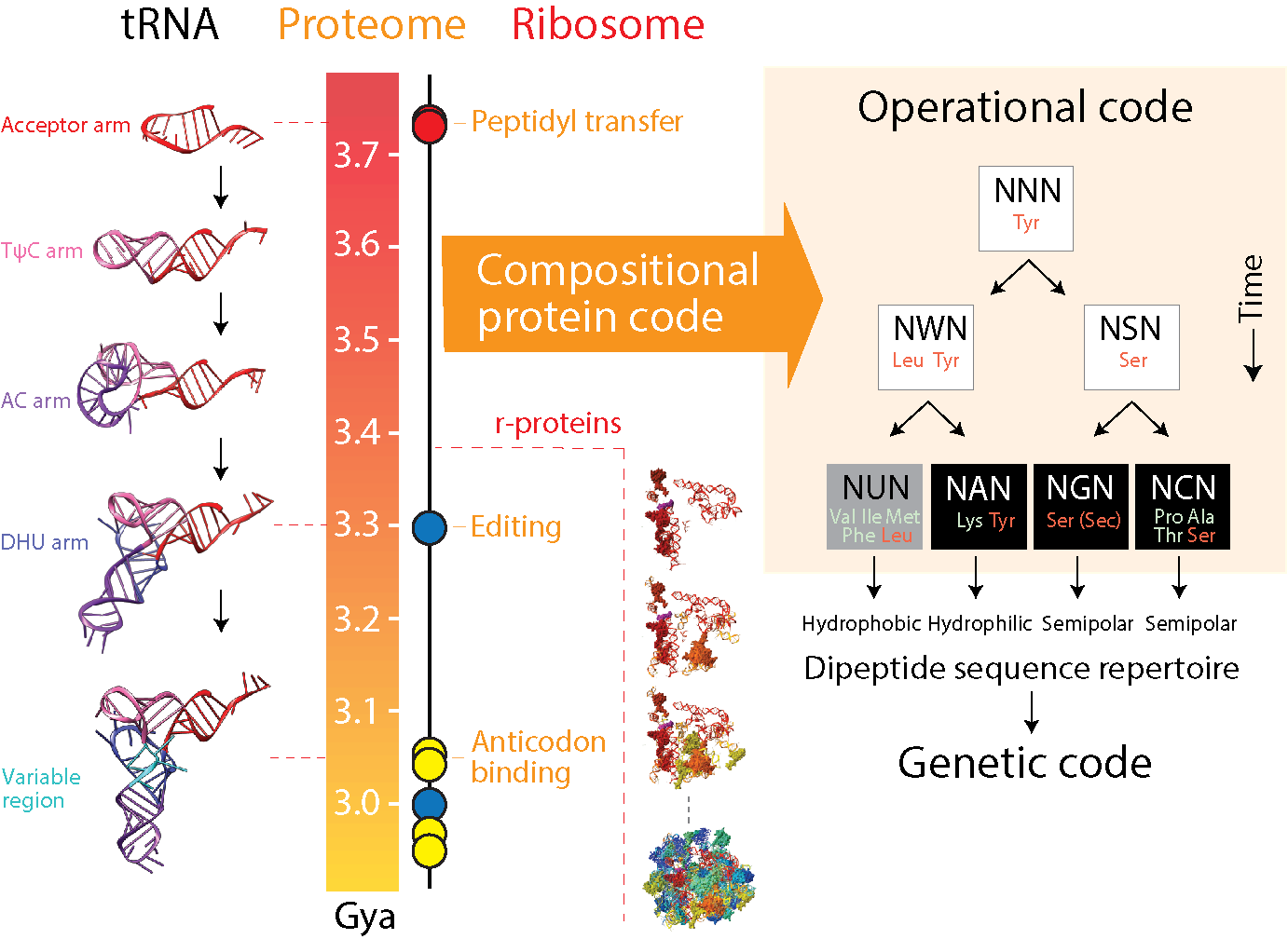
Есть несколько гипотез происхождения генетического кода: замороженная случайность (генетический код возник случайно и в таком виде закрепился, потому что с появлением первых функциональных пептидов любое изменение было бы летальным), коэволюционная теория (код формировался вместе с путями синтеза аминокислот), оптимизация на помехоустойчивость (код продолжал некоторое время изменяться после своего появления, поэтому современный код является лучшим из возможных, обеспечивая максимальную приспособленность и минимизируя последствия мутаций) и стереохимическое сродство (генетический код определяется высоким сродством каждой аминокислоты с соответствующими ей кодонами и антикодонами). Возможно, древние рибозимы, подобные современным тРНК, имели разное сродство к аминокислотам, причём кодоны из разных частей одного и того же рибозима могли обладать наибольшим сродством к разным аминокислотам. Сродство аминокислоты и антикодона означает, что предковым тРНК соответствовали те аминокислоты, с которыми они связывались с наибольшим сродством. В ходе эволюции соответствие антикодонов и аминокислот заменилось соответствием аминоацил-тРНК-синтетаз и аминокислот.
Если бы соответствие между кодонами и аминокислотами было случайным, в природе существовало бы 1,5 × 1084 генетических кодов – столько же, сколько есть способов разложить 21 предмет (20 кодонов для аминокислот и один стоп-кодон) в 64 корзины, чтобы каждый предмет был использован по крайней мере единожды. Однако соответствия кодонов и аминокислот неслучайны. Аминокислоты, которые имеют общий путь биосинтеза, как правило, имеют общую первую букву кодонов. Кодоны аминокислот со схожими физико-химическими свойствами, как правило, похожи. Например, вторая буква связана с таким свойством аминокислот, как гидрофобность. Третья буква обычно случайна, её назначение – конденсация ошибок рибосомы. Правдоподобная гипотеза о возникновении должна объяснять такие свойства стандартного генетического кода, как отсутствие кодонов для D-аминокислот, включение всего лишь 20 аминокислот из возможных 64, ограничение синонимичных замен третьей позицией кодонов, функционирование в качестве стоп-кодонов именно кодонов UAG, UGA и UAA и т.д.
Согласно гипотезе неоднозначных пар оснований, выдвинутой ещё в 60-е гг. Фрэнсисом Криком, трёхбуквенный код ДНК произошёл от более простой двухбуквенной системы, используемой примитивными РНК на заре развития жизни. Уже при первом взгляде на таблицу генетического кода можно увидеть закономерность: первые две буквы кодонов обычно кодируют одну и ту же аминокислоту, а третья буква в таком случае является избыточным элементом, предохраняющим от ошибок. В 2005 г. учёные из университета города Бат (Великобритания) Стефан Бэгби, Ян ван ден Эльсен и Хуан-Лин Ву реконструировали этот древний код и нашли объяснение избыточности современного кода ДНК. Возможно, ранние формы жизни имели в распоряжении всего 16 аминокислот, и этим аминокислотам соответствовали 16 вариантов (из 4-х по 2) двухбуквенных кодонов, которые читались группами по три. На каком-то этапе произошла мутация, сделавшая кодоны трёхбуквенными и позволившая включить ещё пять аминокислот. Поскольку две из новых аминокислот (глутаминовая и аспаргиновая) неустойчивы к нагреванию, это могло произойти только когда Земля достаточно остыла. Вероятно, уже после кислородной катастрофы 2.5 млрд лет назад, когда изменился состав атмосферы и произошло глобальное оледенение.
Переход от РНК к ДНК как основному носителю генетической информации можно сравнить с появлением компьютеров архитектуры фон Неймана, у которых блок памяти для хранения инструкций и данных отделён от центрального процессора, обрабатывающего данные по инструкциям. ДНК в данной аналогии является жёстким диском, РНК – оперативной памятью, а рибосома – процессором. РНК делегировала функцию блока памяти молекуле ДНК, у которой нет гидроксильной группы рибозы, что делает её устойчивее к ультрафиолету и не подверженной гидролизу, но лишает каталитической активности. Однако реакция превращения рибозы в дезоксирибозу связана с образованием опасных радикалов, поэтому рибозимы не могут её осуществлять. Реакцию проводят ферменты рибонуклеотидредуктазы – большие белки, для кодирования которых нужны тысячи нуклеотидов. Как же РНК могла эволюционировать в ДНК, если у протоклетки ещё не было полноценной рибосомы для синтеза таких белков?
Здесь нам нужно рассмотреть происхождение внутриклеточного механизма считывания генетического кода – транскрипции. Ключевую роль в процессе транскрипции играют ферменты полимеразы. Современные РНК-полимеразы являются ДНК-зависимыми, т.е. в процессе транскрипции синтезируют РНК на матрице ДНК, но у некоторых вирусов сохранились их предшественники – РНК-зависимые РНК-полимеразы, подозрительно напоминающие фермент теломеразу у эукариотов. Бактериальная РНК‑полимераза работает быстро (порядка десятков нуклеотидов в секунду), но допускает ошибки транскрипции примерно в 1 на 10⁴ нуклеотидов, при этом у неё нет полноценного механизма исправления ошибок, как у ДНК‑полимеразы. В 2020 г. вышла работа группы Евгения Кунина, в которой методами биоинформатики реконструировалась эволюция ДНК и РНК-полимераз. Согласно этим реконструкциям, первой появилась РНК-зависимая РНК-полимераза, от которой потом произошли ДНК-полимеразы. Это в очередной раз указывает, что исторически первым носителем наследственной информации была РНК.
Центральная догма молекулярной биологии запрещает переход информации от РНК к ДНК, но существует процесс обратной транскрипции, который используют в своем жизненном цикле РНК-вирусы. Все известные вирусы являются внутриклеточными паразитами: они проникают внутрь клетки и встраивают в её ДНК свой геном, чтобы перепрограммировать механизмы транскрипции и трансляции на репликацию вируса. Иногда вирусные гены закрепляются в ДНК и даже дают своим носителям полезные адаптации. Согласно основной гипотезе редукции, вирусы произошли путём упрощения первичных клеток, ставших паразитическими. Однако у РНК-вирусов есть несколько эксклюзивных генов и белков, которые отсутствуют у бактерий, архей и эукариотов. Учитывая, что паразитизм является естественным побочным продуктом дарвиновской эволюции, вполне логично предположить, что они возникли вместе с клеточной формой жизни, а может и раньше. Возможно, вирусы стали продуктом коэволюции РНК и пептидов, когда паразитические репликаторы обзавелись белковой оболочкой. А до этого они существовали в виде самореплицирующихся рибозимов, как современные вироиды.
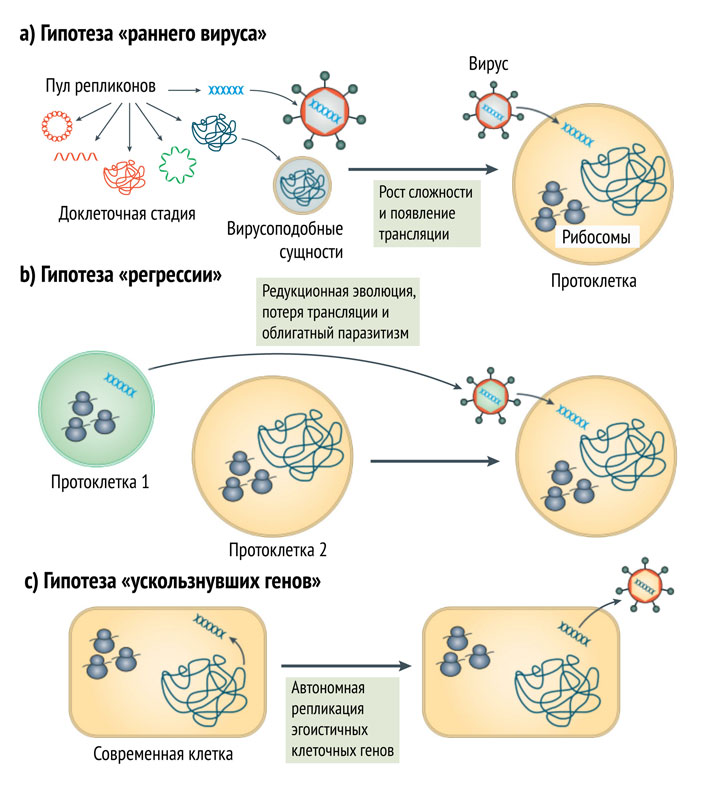
Гипотеза «вирусного мира» идёт ещё дальше и рассматривает доклеточную стадию жизни как пул конкурирующих вирусоподобных репликаторов, обитающих в первичном бульоне, свободно обменивающихся генетическим материалом и не имеющих ни полноценных рибосом, ни независимого метаболизма. Тогда первыми ещё до клеток появились РНК-вирусы, клетки возникли как фабрики и резервуары для производства и распространения вирусов, а потом ретровирусы научились превращать свою РНК в ДНК и эволюционировали в ДНК-вирусы. Французский биолог Патрик Фортер ввёл концепцию вироклетки, чтобы формализовать различие между метаболически инертным внеклеточным вирионом и метаболически активной инфицированной клеткой, утверждая, что последняя представляет собой истинную живую форму вируса. Впоследствии Сахвиндер Гилл и Патрик Фортер расширили модель, предположив, что исходные внеклеточные везикулы могли быть эволюционными промежуточными звеньями между простыми липидными мембранами и первыми вирионами, а ранние рибовироклетки (клетки, одновременно способные делиться и производить вирионы) представляют собой переходную стадию до LUCA. Евгений Кунин также предположил, что вирусные капсиды могли функционировать как примитивный тип компартмента, который помог заложить основы мембранной архитектуры, в конечном итоге принятой клетками.
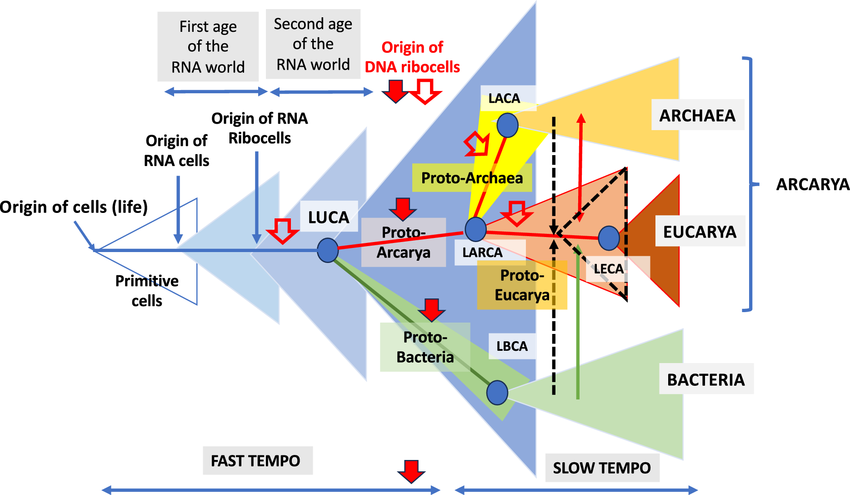
Патрик Фортер также предложил гипотезу вирусного происхождения ДНК: три независимых ДНК-вируса вытеснили исходный геном РНК в трёх отдельных первичных клеточных линиях, дав начало бактериям, археям и эукариотам. Это объясняет отсутствие гомологии между ДНК-полимеразами трёх доменов. Ранние РНК-репликаторы изобрели обратную транскриптазу – белок, синтезирующий РНК на матрице ДНК – а с ним и саму возможность использовать ДНК для хранения информации. Предполагается, что ДНК впервые появилась именно у вирусов как более стабильный геномный материал. В ходе естественного отбора вирусы создавали новые типы нуклеиновых кислот: метил-РНК, урацил-ДНК и современную ДНК с тимином. Совершенствование их копирования во множестве линий вирусов привело к обильному разнообразию ферментов, а выгодой стало прохождение защитных систем клетки. Вирусы начали использовать дезоксирибонуклеотиды и перешли на ДНК в качестве хранителя информации для защиты от клеточных РНК‑репликаз. Позже клетки заимствовали ДНК вместе с ферментами (обратной транскриптазой и рибонуклеотидредуктазами), интегрировав её в собственные геномные системы, чтобы увеличивать их стабильность.
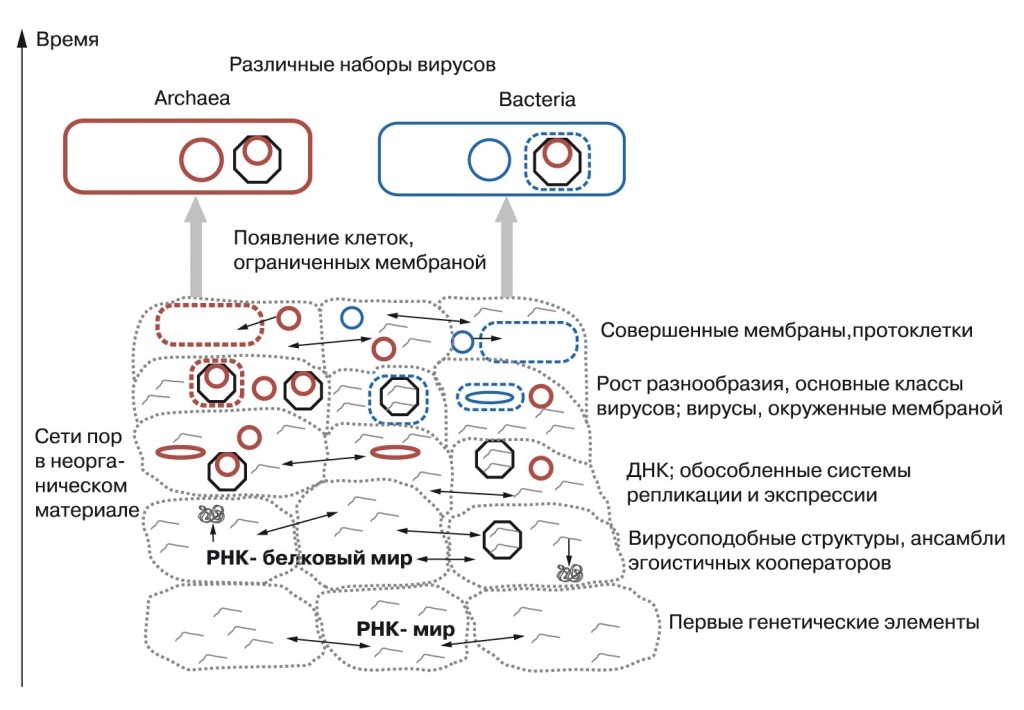
В 2012 г. Джеффри Димер и Кен Стедман из Портлендского государственного университета в Орегоне исследовали вирусы в горячем кислотном озере в Национальном парке вулканов Лассен в Калифорнии и обнаружили доказательства того, что простой ДНК-вирус приобрёл ген от совершенно неродственного РНК-вируса. Вирусолог Луис Вильярреал из Калифорнийского университета в Ирвайне также предполагает, что вирусы, способные преобразовывать ген на основе РНК в ген ДНК, а затем включать его в более сложный ДНК-геном, могли быть распространены в мире вирусов во время перехода от РНК к ДНК около 4 миллиардов лет назад. Это открытие подкрепляет аргумент в пользу передачи информации из мира РНК в зарождающийся мир ДНК ещё до появления последнего универсального общего предка.
Наконец-то, пройдя все этапы абиогенеза, мы пришли к той самой форме жизни, которую искали – бактериальной клетке наподобие LUCA, с генетическим кодом на основе ДНК, механизмами транскрипции и трансляции. Далее на протяжении 2 млрд лет одноклеточная жизнь эволюционировала очень медленно, но она совершила грандиозное по масштабам терраформирование нашей планеты, особенно когда освоила фотосинтез и стала выделять в качестве побочного продукта кислород. Атмосфера остывала и становилась менее плотной, запасы минеральных отложений и органических молекул истощались, а Солнце продолжало светить ультрафиолетом. В таких условиях одни организмы ушли в изолированные, труднодоступные участки, став предками современных архей, населяющих черные курильщики или гейзеры. Другие выбрались на сушу, научились защищаться от солнечного ультрафиолета пигментами, а затем смогли использовать эти пигменты для фотосинтеза, став окончательно независимыми от своей геотермальной прародины. На каком-то этапе они слились с другими бактериями, которые освоили эффективный синтез АТФ из глюкозы и впоследствии стали митохондриями. Ещё одна гибридизация привела к образованию ядра и появлению эукариотов, но это уже другая история.
Вывод
Итак, мы в общих чертах рассказали об абиогенезе – теории возникновения жизни и входящих в её состав органических соединений из неживой и неорганической материи. Мы рассмотрели гипотезы автокаталитических сетей, мира РНК, молекулярного дарвинизма и вирусного происхождения ДНК. Также мы выяснили, кем был последний общий предок и как формировался генетический код. Переход от неживых к живым организмам на Земле был не единичным событием, а процессом возрастающей сложности, включающим формирование пригодной для жизни планеты, пребиотический синтез органических молекул, автокатализ, саморепликацию молекул и появление клеточных мембран. У современных исследователей нет единого мнения о месте возникновения жизни, но диапазон возможных вариантов не так велик: это либо геотермальные источники на дне океана, либо грязевые котлы вблизи вулканов, либо периодически замерзающие и оттаивающие водоёмы. Возможность абиогенного синтеза всех органических молекул, лежащих в основе жизни, уже доказана. Проблема самосборки и саморепликации РНК из нуклеотидов и белков из аминокислот почти решена. Последующие этапы появления генетического кода и механизма трансляции, ДНК, липидных мембран и протоклеток объясняются дарвиновской эволюцией.
Гипотеза мира РНК стала полноценной теорией, достойных конкурентов у неё нет. Теоретически её можно опровергнуть обнаружением необходимого, но совершенно невозможного для земных условий этапа абиогенеза (например, требующего критических температур или давлений, отсутствующих на Земле элементов и т.д.). Вышеперечисленные факты показывают, что принципиальных препятствий для абиогенеза нет. Но достаточно ли всех известных на сегодня фактов, чтобы с уверенностью утверждать, что жизнь возникла именно таким способом? К сожалению, у нас слишком мало информации о распространённости жизни во Вселенной, возможных её формах, условиях ранней Земли и способах абиогенеза, чтобы можно было даже приблизительно оценить вероятность зарождения жизни. Креационисты, которые только и говорят о невероятности абиогенеза, всегда найдут пробелы в теории и примеры «неупрощаемой сложности». Но у них нет собственного объяснения разумного замысла, а именно – конкретного механизма, как Творец создал жизнь сначала в своём разуме, а затем воплотил её в физической форме.
Конечно, лучшим подтверждением возможности абиогенеза стал бы эксперимент в духе Миллера-Юри, в котором прямо в колбе с первичным бульоном в реальном времени возникли бы самовоспроизводящиеся клетки. Но для этого пришлось бы с большой точностью угадать химический состав пребиотической среды и ускорить процесс во много раз, воспроизведя миллионы лет вариации и отбора. И даже если эксперимент увенчается успехом, это будет далеко не факт, что жизнь возникла именно таким способом. В данной статье мы описали наиболее вероятный сценарий зарождения той жизни, которую мы знаем, но нельзя исключать существования альтернативной жизни, образующейся иным путём. Так, исследователь происхождения жизни Пьер Луиджи Луизи из Университета Рома Тре выделяет три её вида: жизнь-какая-она-сейчас, жизнь-какой-она-могла-бы-быть и жизнь-какой-она-когда-то-была. Вполне возможно, что жизнь с другой биохимией или другим генетическим кодом уже неоднократно появлялась на Земле, но не оставила никаких следов, потому что была очень быстро уничтожена более продвинутой доминирующей жизнью. И есть вероятность, что в будущем мы создадим в лаборатории иные формы жизни, которые будут эволюционировать по собственному сценарию.
Завершая статью о происхождении жизни, я надеюсь, что у вас не осталось вопросов по поводу того, как живая материя могла возникнуть из неживой. Жизнь на Земле не является чем-то экстраординарным, она не нарушает законов физики, а сама является закономерным, хотя и не обязательным следствием этих законов. Для её объяснения не нужно прибегать к сомнительным гипотезам о сверхъестественном Творце или о заселении нашей планеты пришельцами. Конечно, ни одна научная теория не может быть доказана на 100%, ведь суть научного метода заключается в постоянной проверке теорий на предмет соответствия фактам. Но на сегодняшний день теорию абиогенеза можно смело поставить в один ряд с теорией эволюции и термодинамикой и заключать пари, что они никогда не будут опровергнуты. Поэтому я закрываю тему происхождения жизни и перехожу к теме происхождения разума. Также в следующих статьях мы рассмотрим космологическую, химическую, биологическую, культурную и техническую эволюции как части единого процесса – универсальной эволюции.
Автор: dionisdimetor


